Dias
Επιφανές μέλος


Dias
Επιφανές μέλος


Dias
Επιφανές μέλος


Dias
Επιφανές μέλος


Δεν είμαι καλός παρηγορητής. Να ακολουθήσεις τη ρήση του Πλούταρχου: "Ο διδάσκων δις διδάσκεται". Να προσπαθήσεις να τα εξηγήσεις σε κάποιον άλλο, π.χ. στο αρκουδάκι σου.Νιώθω ότι δεν θα τα καταλάβω ποτέ.
Dias
Επιφανές μέλος


Για ξεκόλα: (ο τόνος υποχρεωτικός)View attachment 97838
Εδώ έχω κολλήσει διότι δεν ξέρω ούτε τα αρχικά L.
Διδακτορικό στην ώσμωση κάνεις;
Dias
Επιφανές μέλος


Π1V1 + Π2V2 = (n1+n2)RT => Π1V1 + Π2V2 = Π(V1+ V2) =>
Π = (Π1V1 + Π2V2) / (V1+ V2) = 3,67 atm
Dias
Επιφανές μέλος


Dias
Επιφανές μέλος


Dias
Επιφανές μέλος


Προσπάθησε μόνο να τις στείλεις όρθιες και όχι ξαπλωτές.Έχω και άλλες 5 ίσως μέσα στις επόμενες ώρες να στείλω όσες με δυσκολέψουν.
Dias
Επιφανές μέλος


Dias
Επιφανές μέλος


Μη νομίζεις. Και το Φυσικό του ΕΚΠΑ ένα μάθημα Χημείας έχει και αυτό επιλογής.a ωραια , εμεις δεν εχουμε επαφη με φυσικοχημεια αν και θα επρεπε, οποτε μονο υποψιες.
Dias
Επιφανές μέλος


Μην αγχώνεσαι Γιάν²η. Με ωσμωτική πίεση 1/760 atm μια χαρά είναι. Ο τύπος δεν ισχύει για τη συνολική αλλά μόνο για την ωσμωτική. Και το αποτέλεσμα για 1/760 atm μια χαρά βγαίνει.Τζοτζι δεν ειμαι σχετικος με φυσικοχημεια αλλα θα σου ελεγα να ελεγξεις το μεγεθος της πιεσης που θα βαλεις στον τυπο ( ΠV=mRT/Mr) για να βρεις την μοριακη μαζα.
Ποιο θα σου δωσει λογικο αποτελεσμα
η ωσμωτικη πιεση ως 1/760 atm
ή
η ωσμωτικη πιεση ως 760/760+ 1/760 = 761/760 atm
Dias
Επιφανές μέλος


Dias
Επιφανές μέλος


Dias
Επιφανές μέλος


Απάντηση:View attachment 96867
Ερώτηση 18… Σκέφτομαι πως επειδή είναι δεσμός υδρογόνου, έχει να κάνει σίγουρα με αυτό. Απλώς δεν ξέρω πως να το αιτιολογήσω. Η Mr όμως γενικά του HF είναι 20… Έχω μπερδευτεί.
Αφού θέλεις εξήγηση για Μr = 120, τι σε νοιάζει το 240; Μάλλον το HF κάνει εξάγωνο τελικά.
Dias
Επιφανές μέλος


CaCO3 + H2SO4 --> CaSO4 + H2CO3
Αλλάζουν θέση Ca και H2
Όμως το H2CO3 δεν υπάρχει και είναι:
H2CO3 --> H2O + CO2
Dias
Επιφανές μέλος


4,48L = 0,2molΕίναι πολύ απλό, αλλά έχω σπάσει το κεφάλι μου.
CaCO3 + H2SO4 --> CaSO4 + H2O + CO2
..1mol...................1mol.............1mol
.0,2mol................0,2mol...........0,2mol
CaSO4 : 40+32+16.4 = 136
0,2.136 = 27,2g CaSO4
Θέλεις να συνεχίσω;
Dias
Επιφανές μέλος


Είναι. Υπάρχουν στην τράπεζα θεμάτων και σχετικές με τη διαλυτότητα ερωτήσεις σε κάποια 2α θέματα.Η διαλυτότητα είναι πια εντός ύλης?
Σημείωση: Το μήνυμα αυτό γράφτηκε 10 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Θα προσθέσω και κάτι άλλο: Το πεχάμετρο δεν είναι παρά ένα μηχάνημα που δείχνει έναν αριθμό, οπότε είναι κατάλληλο για έναν επαγγελματία που τον ενδιαφέρει μόνον η τιμή του pΗ. Το πεχαμετρικό χαρτί όμως είναι πολύ πιο εκπαιδευτικό μέσο, καθώς βλέπεις την αλλαγή, συγκρίνεις χρώματα και καταλαβαίνεις την έννοια του δείκτη και το μηχανισμό του φαινομένου.5 m όμως είναι υπεραρκετά για μια ερασιτεχνικη χρήση!!!!
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Δες ΕΔΩ ή ΕΔΩ.Ξερει κανεις που θα βρω πεχαμετρικο χαρτι; γιατι ψαχνω στο google και δε βρισκω
Το πεχάμετρο είναι πιο ακριβές, αλλά και πολύ πιο ακριβό (>50€), ενώ το χαρτί από 7,38€.Πάρε πεχάμετρο. Πιο φθηνό και πιο ακριβές είναι (αναλογικά πάντα)

Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Είναι ένα ωραίο ποιηματάκι για την ηλεκτροχημική σειρά.Το θυμάται κανείς;
METAΛΛΑ : K, Ba, Ca, Na, Mg, Al, Mn, Zn, Fe, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, Au
Κάνε βαριά καρδιά ναύτη μάγκα αλλά μην ζητάς φέτος νύφη συνυφάδα πάμπερ. Η Κούλα υδράργυρο αγαπά. Πετάω.
ΑΜΕΤΑΛΛΑ : F2, Cl2, Br2, O2, I2, S
Φάε χυλόπιτα βρωμιάρη όταν είσαι σπίτι

Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


και στον ηλεκτρονιακό τύπο τι γίνεται? μένει ίδιος όπως θα ήταν σε μια απλή ομοιοπολική ένωση?

Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Εχω μια ερωτηση που ηταν στο διαγωνισμα τετραμηνου και μου εσπασε το κεφαλι: Ποιος ειναι ο ατομικος αριθμος του στοιχειου που εχει ενα ζευγος και μηδεν μονηρη ηλεκτρονια στη στιβαδα σθενους?
Και ρωταω εγω τωρα, γινεται ενα στοιχειο να εχει ενα ζευγος και μηδεν μονηρη???? Αφου απο 5 και πανω ηλεκτρονια γινονται ζευγη!!!
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Το θέμα που γράφουμε βρίσκεται στην κατηγορία της Α λυκείου. Σύμφωνα με το βιβλίο της Α λυκείου, η σειρά δραστικότητας των αμετάλλων είναι αυτή που έγραψα.Συγνωμη αλλα η δραστικότητα των αμεταλλων δεν ειναι: F<O<N,Cl<Br<S,C,I<P,Η

Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


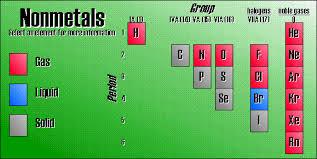
F2 ,Cl2 , Br2 , O2 , I 2, S ---> Φάε χυλόπιτα βρωμιάρη όταν είσαι σπίτι
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Πρέπει να λείπει από την εκφώνηση η περιεκτικότητα του διαλύματος του οξέως (και πρέπει να ζητάει το Mr του μετάλλου και όχι του υδροξειδίου).Ορισμένη μάζα υδροξειδίου δισθενούς μετάλλου Μ εξουδετερώνεται πλήρως από 20 mL διαλύματος HNO3. Το ουδέτερο άλας που προκύπτει ζυγίζει 1,64 g. Να βρείτε την μάζα και το Μr του υδροξειδίου.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Δεννομίζω ότι αυτό για στερεά - αέρια ισχύει. Π.χ.Ενα στερeο η αεριο αντικαταστει ενα στερeο η αεριο αντιστοιχα!
ΠΧ. Υ + ΧΙ --> Χ+ ΥΙ
Το Υ και το Χ ειναι και τα δυο στερeα η αερια.
Zn(s) + 2HCl →ZnCl₂ + H₂(g)
F₂(g) + 2NaI → 2NaF + I₂(s)
s = στερεό, g = αέριο

Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Όξινα λέμε τα οξείδια των αμετάλλων γιατί με νερό δίνουν οξέα, βασικά λέμε τα οξείδια των μετάλλων γιατί με νερό δίνουν βάσεις. Όταν έχεις αντίδραση με οξείδιο, να την κάνεις στο πρόχειρο βάζοντας αντί το οξείδιο, το αντίστοιχο οξύ ή βάση και η διαφορά θα είναι στα νερά. Περισσότερα στο βιβλίο σου, σελίδες 93 και 104.Έχω ακόμα μια απορία οξείδια δεν είναι οι ουσίες που στο μόριο τους έχουν οξυγόνο γιατι χωρίζονται σε όξυνα οξείδια και βασικά οξείδια ??Και όταν λες να κάνω αναγωγή εννοείς να κάνω κανονικά την αντίδραση ?

Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Χε! Εδώ το σχολικό βιβλίο έχει τυπογραφικό λάθος που κανένας δεν βρέθηκε τόσα χρόνια να το διορθώσει. (Το βρήκε πέρυσι η Κατερίνα με τα πολλά ΟοΟοΟοΟ)Η εφαρμοφή λεει:
Ποσο ζυγίζει 1 άτομο υδρογονο αν Ar H = 1
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Τώρα κάνεις παζάρια?...αν πάω Τεχνολογική Κατεύθυνση,χρειάζονται τα 2 πινακάκια αυτά?

Για φέτος Α λυκείου θα σου χρειαστούν και πρέπει να τα μάθεις.
Αν στη Β πας τεχνολογική και στη Γ πας τεχνολογική (2ο κύκλο), του χρόνου μπορείς να τα ξεχάσεις.
Αν όμως στη Γ πας τεχνολογική 1ο κύκλο?
ΕΣΥ αποφασίζεις!!!
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Ότι και να σου πει ο καθηγητής σου (π.χ. ίσως, αργότερα, κάποια στιγμή) εσύ (ειδικά αν θα ακολουθήσεις θετική):...το βιβλιο της Α' Λυκειου εναν πινακα που ειχε με αριθμο οξειδωσης και εναν αλλον με ονοματολογια κυριοτερων πολυατομικων και μονοατομικων ιοντων πρεπει να τους μαθω?
Τους αριθμούς οξείδωσης των στοιχείων και τα πολυατομικά ιόντα (όνομα και αριθμό οξείδωσης), πρέπει οπωσδήποτε να τα μάθεις απέξω και ανακατωτά. Θα σου χρειάζονται συνέχεια.
Γράψε τα πινακάκια σε χαρτόνι 2 φορές. Το ένα θα το κολλήσεις στο γραφείο σου και το άλλο (αν μπορείς πλαστικοποιημένο) θα το έχεις πάντα μέσα στο βιβλίο της χημείας.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Θα προσπαθήσω.το διαβασα αλλα δεν το καταλαβαινω. μπορεις να μου το εξηγησεις σε παρακαλώ?
Τα οξέα περιέχουν υδρογόνο (Π.χ. ΗCl, HCN). Όταν διαλυθούν στο νερό παθαίνουν διάσταση σε ιόντα: κατιόν Η⁺ και το υπόλοιπο ανιόν (⁻). Οι ιδιότητες των οξέων οφείλονται στο Η⁺. Σε άλλα οξέα όλα τα μόρια παθαίνουν διάσταση (Π.χ. ΗCl → H⁺ + Cl⁻) οπότε παρουσιάζουν έντονα τις όξινες ιδιότητες και λέγονται ισχυρά. Ενώ σε άλλα μικρό μόνο μέρος των μορίων παθαίνει διάσταση (Π.χ. HCN ⇋ H⁺ + CN⁻), δηλαδή στο διάλυμα υπάρχουν και ιόντα H⁺ , CN⁻ και μόρια HCN αδιάστατα, έτσι οι όξινες ιδιότητες παρουσιάζονται χαλαρά και τα οξέα αυτά λέγονται ασθενή.
Απαντώ στο παρακάτω μήνυμα (Μη χαλάσω από τώρα το 1000)
Δεν μιλάμε για μέρος του μορίου, αλλά του συνόλου των μορίων. Από όλα τα μόρια του ΗCN που ρίχνουμε στο νερό, ένα μέρος (π.χ. το 10% των μορίων) παθαίνει διάσταση σε ιόντα H⁺ , CN⁻ και τα υπόλοιπα (π.χ. 90%) μόρια παραμένουν αδιάσπαστα μόρια HCN.ποιο μερος του HCN δεν παθαινει διασταση? το CN?

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Βιβλίο σελ. 85.αυριο γραφω χημεια και εχω μια απορία μπορει να με βοηθήσει καποιος(το συντομοτερο δυνατον)? μπορειτε να μου εξηγήσετε τη διαφορά μεταξύ ισχυρού και ασθενoύς οξέος?
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Επιτέλους δικαιώθηκα. Τωρα να μου φύγει και το άγχος και μια χαρούλα!!!!!!!!

 Συγχαρητήρια!!! (Χάνεις όμως πόντους από την ασαφή διατύπωση της απορίας).
Συγχαρητήρια!!! (Χάνεις όμως πόντους από την ασαφή διατύπωση της απορίας). Να και μια "ασκησούλα" για όσους είναι Α λυκείου και δίνουν Χημεία κατάλληλη για θέμα:
Να και μια "ασκησούλα" για όσους είναι Α λυκείου και δίνουν Χημεία κατάλληλη για θέμα: - Διαθέτουμε διάλυμα Α νιτρικού οξέος 2Μ και διάλυμα Β νιτρικού οξέος 3,15% w/v.
α) Ποιο από τα δύο διαλύματα είναι πυκνότερο;
β) Πόσα mL ενός από τα δύο διαλύματα πρέπει να αραιώσουμε με νερό, ώστε να προκύψουν 500mL διαλύματος Γ 0,6Μ;
γ) Εάν αναμίξουμε 100mL του διαλύματος Α και 400mLτου διαλύματος Β, πόση θα είναι η μοριακότητα κατʼ όγκο του διαλύματος Δ που θα προκύψει;
δ) Πόσος όγκος υδατικού διαλύματος υδροξειδίου του ασβεστίου 0,05Μ απαιτείται για την πλήρη εξουδετέρωση του παραπάνω διαλύματος Δ;
Καλές λύσεις...............................................................

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Χα!!!! Έχεις δίκιο!!!! (Τώρα κατάλαβα τι θέλεις, ως τώρα δεν ήσουν σαφής).Eντάξει αυτό με το θείο το ξεκαθάρισα. Μπορεί να μου λύσει κάποιος την άλλη απορία που δεν θα κοιμηθώ αν δεν το βρω!
Λοιπόν: 1/ΝΑ = 1,66‧10 ˉ²⁴ g !!!!!! Και τόση είναι στα αλήθεια η μάζα του πρωτονίου.
Άρα το βιβλίο έχει λάθος!!!!!

Και τώρα μπορείς να κοιμηθείς ήσυχα (και απονήρευτα ε?
 )...
)...
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


O A.O. του ιόντος SO3= είναι -2 και όχι -1.2) Άμα το θειώδες είναι ιόν και π.χ θέλω να βρω τον Α.Ο του θείου δεν είναι 1*χ+3*(-2)=-1
Ξέρεις πώς λέγεται αυτό που κάνεις μόνη σου? (ξέρεις...1) Ναι αλλά το ΝΑ είναι 6,02*10 στην 23. Αυτός με αυτό διαιρεί και βγαίνει 1,66* 10 στην -23; Εγώ που το κάνω μόνη μου το βγάζω 1/6,02* 10 στην -23. Είναι σωστό έτσι;
 ). Θεωρείς δεδομένο το αποτέλεσμα και υπολογίζεις το ΝΑ.
). Θεωρείς δεδομένο το αποτέλεσμα και υπολογίζεις το ΝΑ.Ο πλανήτης πήρε το όνομα του από το θεό...Υ.Γ. Ναι αλλά εσύ στην εικόνα έχεις τον Θεό όχι τον πλανήτη!

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


1) Μα... με το ΝΑ διαιρεί. Το άλλο είναι το αποτέλεσμα που βγαίνει.1) σελ131 βιβλίου. Ρωτά πόσο ζυγίζει το 1 άτομο υδρογόνου. Γιατί διαιρεί στην λύση με 1,66*10 στην -24 και όχι με το ΝΑ που είναι 6,02*10 στην 23;
2) Επίσης μια άλλη απορία μου σχετικά με τον Α.Ο. του SO3. To παίρνω σαν ρίζα ή κανονικά σαν ένωση για να το βγάλω; Απ ότι κατάλαβα το παίρνω σαν ένωση γιατί το θείο θα χει στάνταρ Α.Ο με βάση το πινακάκι της σελ του μαθήματος. Αν το πάρω σαν ρίζα βγαίνει 5. Αλλά το θειώδες πάντα με προβλημάτιζε γιατί για να λέγεται θειώδες δεν είναι το προηγούμενό του το θειικό που είναι ρίζα με -1; Τι είναι βρε παιδιά γιατί πολύ με ζορίζει αυτό το θειώδες. Το ξέρω ότι λέγεται και τριοξείδιο του θείου, αλλά μπορεί κανείς να απαντήσει, αν είναι ρίζα ή απλή ένωση;
2) Άλλο το θειώδες (το λέμε έτσι γιατί έτσι το βάφτισε η νονά του η IUPAC) ιόν SO3= (όπου το S έχει Α.Ο. +4 και όχι 5) και άλλο το τριοξείδιο του θείου (της θειάς του) SO3 (όπου το S έχει Α.Ο. +6). Μην ανησυχείς και δεν θα μπερδευτείς, θα σου το έχουν ξεκαθαρίσει για ποιο θα μιλάνε. Πάντως το τριοξείδιο του θείου SO3 υπάρχει πραγματικά στη φύση, ενώ το ιόν SO3= (και όλα τα άλλα πολυατομικά ιόντα) είναι μάλλον υποθετικά.

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Μου αρέσει πολύ η χημεία αλλά μου αρέσει πολύ περισσότερο η φυσική.Dia έχω μια ερωτησούλα λίγο οφ τόπικ.... Σκοπεύεις να ασχοληθείς με την χημεία?
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


α) n = C.V = 0,6mol H2SO4 = 58,8g1) Κατά την αραίωση 300ml ενός διαλύματος Δ1 H2SO4 (C=2M) με 200ml νερού προέκυψαν 500ml διαλύματος Δ2
α) πόσα g H2SO4 περιέχονται στο διάλυμα Δ1???
β) ποια είναι η % w/v περιεκτικότητα του διαλύματος Δ2??
γ) Με πόσα ml νερού πρέπει να αραιωθούν 50ml του διαλύματος Δ2 ώστε να προκύψει διάλυμα Δ3 με συγκέντρωση C3=0,5M??
β) Σε 500mL δ/τος περ. 58,8g H2SO4 στα 100mL? => 11,7 % w/v
γ) C1V1 = C2V2 => C2 = 1,2M , C2V2 = C3V3 => V3 = 120mL , VH2O = 70mL
α) C1V1 + C2V2 = C.V , V1 + V2 = V , (σύστημα) => V1 = 240mL , V2 = 480mL2) Διαθέτουμε δύο διαλύματα H2SO4 συγκεντρώσεων 0,5Μ και 2Μ
α) Πόσα ml από το κάθε από αυτά τα διαλύματα πρέπει να αναμείξουμε για να παρασκευάσουμε 600ml διαλύματος C=1M??
β) Πόσα ml ενός από τα δύο διαλύματα που διαθέτουμε πρέπει να αραιώσουμε για να παρασκευάσουμε 400ml ενός άλλου διαλύματος συγκέντρωσης 1.5Μ???
β) Το δεύτερο: C2V2 = C3V3 => V2 = 300mL
α) Σε 180+40 = 220g δ/τος περ. 40g NaOH, σε 100mL? => 18,18 % w/w3) Σε 180g νερού δίνονται 40g NaOH οπότε προκύπτει διάλυμα Δ με πυκνότητα 1,1g/ml
α) Να υπολογιστεί η % w/w περιεκτικότητα και η συγκέντρωση του διαλύματος Δ
β) Πόσα ml νερού πρέπει να προσθέσουμε σε 100ml του διαλύματος Δ ώστε να προκύψει διάλυμα 1Μ??
n = m/Mr = 1mol NaOH , d = m/V => V = 200mL δ/τος , C = n/V = 5M
β) C1V1 = C2V2 => V2 = 500mL => VH2O = 400mL
Το β γιατί προφανώς πρέπει: C1 < C < C24) αναμειγνύουμε διάλυμα H2SO4 (C1=0,5M) με διάλυμα H2SO4 συγκέντρωσης C2, οπότε προκύπτει διάλυμα C=0,8M. Για την
συγκέντρωση C2 ισχύει:
α) C2=0,3M, β) C2 > 0,8M, γ) C2 < 0,8M ή δ) 0,5Μ < C2 < 0,8M

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Κάπου χρειάζεσαι λίγο διάβασμα θεωρίας. Λοιπόν:Είμαστε στοιχειομετρία και ο χημικός μας έβαλε κάτι προβλήματα που αν και τα κατάλαβα στην τάξη εδώ μπλέκουν κάτι με stp που με αποσυντονίζουν τελείως ενώ χρησιμοποιούσαμε καταστατική εξίσωση.
1) Αυτό που πάντα ισχύει είναι ότι:
1mol μορίων ζυγίζει Μr (g) περιέχει ΝΑ μόρια και έχει όγκο 22,4L (αν είναι αέριο και σε stp).
2) Αυτά γίνονται και τύποι:
4) To stp μην σε μπερδεύει. (Εννοεί Ρ = 1atm και Τ = 273Κ). Στο λέει για να σου πει ότι Vm = 22,4L. (Αν δεν είναι stp θέλει καταστατική εξίσωση).
5) Ο γραμμομοριακός όγκος είναι ίδιος για όλα τα αέρια.
6) Ίσοι όγκοι αερίων στις ίδιες συνθήκες περιέχουν τον ίδιο αριθμό μορίων άρα και mol. Δηλαδή η αναλογία όγκων και mol είναι η ίδια.
7) Με αυτά και λίγο διάβασμα από το βιβλίο δεν θα έχεις πρόβλημα.

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Αν έχεις κάποια ερώτηση και ξέρω ευχαρίστως να σε βοηθήσω. Έτσι γενικά τι μάθημα να σου κάνω?ερώτηση->DIΑ πότε θα μου κάνεις μάθημα??!?!?!?!?!?!? βοήθεια παιδιά γιατί καίγομαι!!!!! SOS

Υ.Γ. και μη νομίζεις ότι τα ξέρω όλα. Για ΄παράδειγμα αυτά που λέει ο φίλος για αριθμούς οξείδωσης και ηλεκτρόνια μου είναι σουαχίλι.

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Dia σου χω νέα!!!!! Και καλά!!! Πολύ καλά!!! Γράψαμε διαγώνισμα χημεία κι έγραψα 20!!!!!!!!!!!!!!!!!!!!!!
 Μόνον 20? Ντροπή σου!!!!
Μόνον 20? Ντροπή σου!!!! 
Υ.Γ.



 .......................
.......................

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Στο βιβλίο χημείας Α σελ.12 γράφει ότι το S έχει ατομικότητες 2 ή 4 ή 6 ή 8. Λέει ακόμα ότι στις χημικές εξισώσεις γράφεται σαν μονοατομικό. Φαντάζομαι ότι το γράφουμε έτσι γιατί δεν μπορούμε να ξέρουμε κάθε φορά τι να το βάλουμε. Ακόμα υπάρχει και κρυσταλλικό θείο.Το θείο όταν βρίσκεται σε ελεύθερη κατάσταση γιατί δεν σχηματίζει ομοιοπολικό δεσμό και γίνεται S2; Γιατί σε μια εξίσωση το έγραψα S2 και μου το πήρε λάθος και μου είπε ότι γίνεται σκέτο S. Γιατί όμως δεν υπάρχει αμοιβαία συνεισφορά ηλεκτρονίων και δεν σχηματίζει ένα διατομικό μόριο θείου με διπλό ομοιοπολικό δεσμό;

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Pb(NO3)2 + Na2S = PbS + 2NaNO3
Γιατί μας είπε ότι γίνεται ενώ στο βιβλίο δεν είναι κανένα από τα δύο ιζήματα;;;;;;
 Ουφ!!! Δύσκολο να είσαι θεός!!! Εδώ όμως η απάντηση είναι εύκολη:
Ουφ!!! Δύσκολο να είσαι θεός!!! Εδώ όμως η απάντηση είναι εύκολη: Αν διαβάσεις με προσοχή το πινακάκι ιζημάτων του βιβλίου σου θα δεις ότι λέει ότι:
Αν διαβάσεις με προσοχή το πινακάκι ιζημάτων του βιβλίου σου θα δεις ότι λέει ότι:ΙΖΗΜΑΤΑ: ..............................
Όλα τα θειούχα άλατα εκτός από K2S, Na2S, (NH4)2S.
 Δηλαδή το PbS είναι μια χαρά ίζημα άρα η αντίδραση σου γίνεται και παραγίνεται!!! (αλλά εσύ είσαι απρόσεκτη)
Δηλαδή το PbS είναι μια χαρά ίζημα άρα η αντίδραση σου γίνεται και παραγίνεται!!! (αλλά εσύ είσαι απρόσεκτη) 

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


1. πεντοξείδιο του φωσφόρου + υδροξείδιο του καλίου
2. Τριοξείδιο του θείου + υδροξείδιο του αργιλίου
5.νιτρικό οξύ +οξείδιο του σιδήρου(III)
Θεέ πλιζζζζζ βοήθα!!!

 Δίας: ο από μηχανής θεός?
Δίας: ο από μηχανής θεός?

 Το θέμα είναι να καταλάβεις το μηχανισμό. Όταν έχουμε οξείδιο + οξύ ή βάση βρίσκεις ποιας βάσης ή οξέως είναι ανυδρίτης το οξείδιο και κάνεις εξουδετέρωση.
Το θέμα είναι να καταλάβεις το μηχανισμό. Όταν έχουμε οξείδιο + οξύ ή βάση βρίσκεις ποιας βάσης ή οξέως είναι ανυδρίτης το οξείδιο και κάνεις εξουδετέρωση. P2O5 ανυδρίτης του Η3ΡΟ4
SO3 ανυδρίτης του H2SO4
Fe2O3 ανυδρίτης του Fe(OH)3
 Να και οι αντιδράσεις σου:
Να και οι αντιδράσεις σου:P2O5 + 6ΚΟΗ ---> 2Κ3PO4 + 3H2O
3SO3 + 2Al(OH)3 ---> Al2(SO4)3 + 3H2O
6HNO3 + Fe2O3 ---> 2Fe(NO3)3 + 3H2O
(και συγνώμη που άργησα - είχα πάει βόλτα - δεν θα το ξανακάνω
 )
)Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Σελ.103 κάτω από τον πίνακα με τα αέρια και τα ιζήματα:Σε ποια σελίδα το γράφει;;;;
Παρατήρηση:
Το ανθρακικό οξύ (Η2CO3) και το θειώδες οξύ (H2SO3) είναι ασταθείς ενώσεις, ενώ το υδροξείδιο του αμμωνίου (ΝΗ4ΟΗ) είναι μόριο υποθετικό.

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Mα γιατί;;; Αφού ο θειώδης ή γενικά το θειώδες δεν ακολουθεί τον τύπο του υπερχλωρικού, χλωρικού, χλωριώδους(ClO2), υποχλωριώδους;;; Γιατί το θειώδες δεν θα πάρει δείκτη 2 αφού είναι σαν το χλωριώδες;;;;;;
 Το SO3 = θειώδες γιατί έτσι το βαφτίσανε. Δες το βιβλίο σου!!!
Το SO3 = θειώδες γιατί έτσι το βαφτίσανε. Δες το βιβλίο σου!!!

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Έχεις κάνει λάθος. Δεν υπάρχει ZnSO2 .Toσημαίνει ότι την έχω λάθος ή ότι δεν γίνεται;
O θειώδης ψευδάργυρος είναι ZnSO3 .
ZnSO3 + Na2SO4 = OXI
ZnSO3 + H2SO4 = ZnSO4 + H2O + SO2
Αποφάσισε τι θέλεις!!!

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


2Al +3S =Al2S3M πορεί κάποιος να ελέγξει αν είναι σωστές οι παρακάτω ασκήσεις;
Ας τις δει κάποιος γιατί τις έκανα πολύ βιαστικά και δεν τις πολυκατάλαβα!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
4Al +3O2= 2Al2O3
2Fe+3Cl2=2FeCl3
2Sn +O2=2SnO
2CuO = 2Cu + O2
2AgBr = 2Ag +Br2
Zn + 2HBr =ZnBr2 +H2
I2 + NaF = OXI
3Na + AlCl3 = 3NaCl + Al
3Cu + 2Ag3N = Cu3N2 +6Ag
Ag +HCl = oxi
6K +2H3PO4= 2K3PO4 +3H2
Ba + 2H2O = Ba(OH)2 + H2
Zn + H2O = ZnO + H2
AlCl3 + 3AgNO3 = 3AgCl + Al(NO3)3
BaCO3 + 2HCl = H2O + CO2 + BaCl2
ZnSO2 ?????? + H2SO4 =

Ba(NO3)2 + Na2SO4 = BaSO4 + 2NaNO3
2NH4Cl + Mg(OH)2 = MgCl2 + 2NH3 + 2H2O

NaHCO3 + HI = NaI + CO2 + H2O
(NH4)2SO4 + 2KOH = K2SO4 + 2NH3 + 2H2O
Pb(NO3)2 + Na2S = 2NaNO3 + PbS

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


Αυτός είναι ένας εμπειρικός κανόνας της ανόργανης χημείας: η ένωση συνήθως προκύπτει με τους πιο απλούς δείκτες. Αυτό θα το καταλάβεις καλύτερα κάνοντας ηλεκτρονιακούς τύπους. Φυσικά υπάρχουν εξαιρέσεις π.χ. το υπεροξείδιο του υδρογόνου (Η2Ο2). Επίσης η απολοποίηση δεν γίνεται στην οργανική π.χ. αιθάνιο (C2Η6 δεν θα γίνει CH3). Δέξου τον εμπειρικό κανόνα της απλοποίησης για οξέα-βάσεις-άλατα-οξείδια που μάλλον προέκυψε και από πειράματα. Η χημεία γενικά είναι εμπειρική επιστήμη και πολλά τα δεχόμαστε επειδή είναι πειραματικά δεδομένα.υπαρχει λογος που απλοποιείται ο λογος ψ/χ στις ενωσεις?(οι δεικτες, οταν ΑψΒχ) πχ το P4O10 συμφωνα με το βιβλιο μπορει να γινει P205 .γιατι γινεται αυτο το πραγμα δεν αλλαζει ολο το στοιχειο με αυτον τον τροπο?
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


METAΛΛΑ : K, Ba, Ca, Na, Mg, Al, Mn, Zn, Fe, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, AuΕίμαστε στις κατηγορίες αντιδράσεων. Μπορεί να γράψει κανείς ποιηματάκια δραστικότητας των μετάλλων και αμετάλλων για να τα μάθω πιο εύκολα. Άκουσα ένα και βάσανα μεγάλα αλλά παρακάτω δεν το θυμάμαι;;;;....
Κάνε βαριά καρδιά ναύτη μάγκα αλλά μην ζητάς φέτος νύφη συνυφάδα πάμπερ. Η Κούλα υδράργυρο αγαπά. Πετάω.
ΑΜΕΤΑΛΛΑ : F2, Cl2, Br2, O2, I2, S
Φάε χυλόπιτα βρωμιάρη όταν είσαι σπίτι

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


γεια σας. υπαρχουν αρκετα πραγματα που δεν εχω καταλαβει απο την παραγραφο 2.4 του βιβλιου....
 Τις απαντήσεις στις απορίες σου θα τις λύσεις πολύ εύκολα αν διαβάσεις πολύ καλά το βιβλίο και κάνεις όλα τα παραδείγματα αλλά όχι κοιτάζοντας τα μόνον αλλά γράφοντας. Αν έχεις και κάποιο βοήθημα κάνε και άλλα παραδείγματα απο κει. Διαφορετικά ότι και να σου πουμε εδώ δεν λέει τίποτα.
Τις απαντήσεις στις απορίες σου θα τις λύσεις πολύ εύκολα αν διαβάσεις πολύ καλά το βιβλίο και κάνεις όλα τα παραδείγματα αλλά όχι κοιτάζοντας τα μόνον αλλά γράφοντας. Αν έχεις και κάποιο βοήθημα κάνε και άλλα παραδείγματα απο κει. Διαφορετικά ότι και να σου πουμε εδώ δεν λέει τίποτα. Και μια δική μου απορία: είσαι Β λυκείου όπως γράφεις? Αν ναι γιατί θυμήθηκες τώρα τη χημεία της Α?
Και μια δική μου απορία: είσαι Β λυκείου όπως γράφεις? Αν ναι γιατί θυμήθηκες τώρα τη χημεία της Α? 
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Dias
Επιφανές μέλος


NaHCO3 + HI ---> NaI + H2O + CO21) όξινο ανθρακικό νάτριο+υδροιώδιο
2) νιτρικό βάριο+θειικό νάτριο
3) ανθρακικό βάριο+υδροχλώριο
Ba(NO3)2 + Na2SO4 ---> BaSO4 + 2NaNO3
BaCO3 + 2HCl ---> BaCl2 + H2O + CO2

Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
-
Το forum μας χρησιμοποιεί cookies για να βελτιστοποιήσει την εμπειρία σας.
Συνεχίζοντας την περιήγησή σας, συναινείτε στη χρήση cookies στον περιηγητή σας.
 Αρχική Forum
Αρχική Forum
 Ρωτήστε κάτι
Ρωτήστε κάτι
 Προσωπικές Συζητήσεις
Προσωπικές Συζητήσεις
 Πανελλαδικές
Πανελλαδικές
 Αγγελίες
Αγγελίες
 Συνδεδεμένοι Χρήστες
Συνδεδεμένοι Χρήστες
 Λίστα Αποκλεισμένων
Λίστα Αποκλεισμένων
 Υπεύθυνοι του Forum
Υπεύθυνοι του Forum
 e-steki
e-steki

