Chemwizard
Τιμώμενο Μέλος


Chemwizard
Τιμώμενο Μέλος


Chemwizard
Τιμώμενο Μέλος


Μια επισύμανση: οι 1,2,3.. είναι στιβάδες. Οι s, p, d είναι υποστιβάδες. Όσον αφορά τις υποστιβάδες, ισχύει αυτό που λες. Όσον αφορα τις στιβάδες, είναι το άθροισμα των υποστιβαδων. Η 1 δηλαδή χωράει 2 ηλεκτρονια, η 2 χωράει 8 κοκ.Α ενταξειτοτε ναι ο εκθέτης στην στιβάδα s δειχνει πόσα ηλεκτρόνια μπορούν να τοποθετηθουν δηλαδή 2.
Στην στιβάδα p μπορούν 6e,στην στιβάδα d 10e κι στην f 14e.
Σημείωση: Το μήνυμα αυτό γράφτηκε 5 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Το ms=-1/2 δεν συμμετέχει στη διαμορφωση της τιμής του ηλεκτρονιου ούτε στον καθορισμό του τροχιακου αλλά καθορίζει την ιδιοπεριστροφη του ηλεκτρονιου.Στη συγκεκριμένη περίπτωση επειδή είναι αρνητικό δείχνει ότι έχουμε αντιπαραλληλο spin ή spin προς τα κάτω.Ουτε το αφαιρεις ούτε το προσθέτεις.Λογικα θα εννοείς ml=-1 όπου το ml παίρνει τιμές από -l,...,+l κι δείχνει τον προσανατολισμό του ηλεκτρονιακου νέφους.Για τα p ατομικά τροχιακά πχ(n,,l=1 και ml=-1,0,+1) αντιστοιχούν 1 υποστιβαδα(l) κι 3 τροχιακα(ml).Το άλλο δεν κατάλαβα το 2 τι ειναι στο 1s2
Μάλλον το 2 είναι εκθέτης κι εννοει τα 2 ηλεκτρόνια του 1s.
Σημείωση: Το μήνυμα αυτό γράφτηκε 5 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Να δοθεί εξήγηση στην παρακάτω πρόταση "οι πυρκαγιές στους αλευρόμυλους έχουν πολύ μεγάλες ταχυταχύτες"αυτό γιατί συμβαίνει; μπερδευομαι γιατί τα αλευρα είναι σε μορφή σκόνης κι άρα θα έχουν μικρότερη επιφάνεια επαφής επομένως δεν θα εχουν ελαττωση της ταχύτητας;
Ξανασκέψου το.
1 τουβλο ενα κιλο κι ενα κιλο σκονης. Που εχεις τη μεγιστη συνολικη επιφάνεια;
Σημείωση: Το μήνυμα αυτό γράφτηκε 5 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


https://www.kelafas.gr/themata.html?filename=2013/epanaliptikes/chem_epan_2013_e.pdf
Το Α4
τωρα μολις σκεφτηκα οτι αν κανω τον ιοντισμο της CH3NH2 ειναι βασικο αρε με την προσθηκη νερου μειωνετε το pH,τεινει προς το 7 αρα τα ΟΗ μειωνονται ....σωστα η λεει χαζομαρες βραδιατικα?
Με την ερώτηση που ειδα άλλαζει το πραγμα. Δεν προσθετεις νερο σε μεθυλαμινη αλλα αραιωνεις υδατικο διαλυμα μεθυλαμινης. Κι αφου η μεθυλινη εδινε OH-, πεφτει κι η δική τους συγκέντρωση.
Θεμα διατυπωσης σου.
Σημείωση: Το μήνυμα αυτό γράφτηκε 5 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Γιατι κατα την προσθηκη νερου σε CH3NH2 το [ΟΗ]-ελαττωνεται ???
Που το ειδες αυτο;
Κατ'αρχην CH3NH2 προσθετεις σε νερο κι οχι το ανάποδο.
Κατα δευτερον αυτο είναι μεθυλαμινη, αρα το pH ανεβαινει.
Σημείωση: Το μήνυμα αυτό γράφτηκε 5 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Καλησπέρα! Γνωρίζει κανείς κάποιο site με βιντεάκια, σημειώσεις, ασκήσεις , διαγωνίσματα κτλ ; Δίνω του χρόνου πανελλήνιες θετική και επειδή δεν θα κάνω φροντιστήρια, προσπαθώ να μαζέψω όσο περισσότερο υλικό μπορώ. Ευχαριστώ εκ των προτέρων.
ylikonet.gr
Μετά ψάχνεις ανα κεφάλαιο τι σε ενδιαφέρει.
Να θυμάσαι όμως: δυστυχώς, στις Πανελλήνιες δε μετρά μόνο οι γνώσεις που έχεις, αλλά και πόσο καλα έχεις φωτοτυπησει το μυαλό σου το σχολικό βιβλίο.
Μη φύγεις παραπέρα χωρίς να κάνεις αυτό κτίμα σου πρώτα.
Οτιδήποτε αλλο χρειάζεσαι, εδώ υπάρχει κόσμος για συζήτηση και βοήθεια.
Ακριβώς για τον ίδιο λόγο με εσένα είχε φτιάξει κι ο @Scandal το φόρουμ.
Σημείωση: Το μήνυμα αυτό γράφτηκε 5 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος



Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Ka 1,2 οι σταθερές των συζυγών οξέος - βάσης.
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Τώρα το είδα.οταν κορεσμενη μονοσθενης αλκοολη μετατραπει σε καρβονυλικη ένωση παρουσιάζει ελάττωση βάρους 2,7 %. αν δίνει αλογονοφορμικη να βρειτε το συντακτικο τυπο της αλκοοολης

Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


επομένως, ισχύει οτι η ενέργεια πρωτου που απαιτει το μαγνησιο είναι μεγαλύτερη;
Ναι, δεν το βλέπεις και στην εικόνα πριν το Al?
Aν παρατηρήσεις, τα σκαλοπατάκια που πέφτουν λίγο και χαλάνε τις ανηφόρες, είναι άτομο μετά από άλλο άτομο που έχει κάτι συμπληρωμένο.
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Η συγκριση ειναι με το 13ΑL , η απάντηση όμως παραμένει η ίδια. Έτσι; Δηλαδή παρα το γεγονός ότι το 13 AL έχει πιο δραστικό πυρηνικό φορτίο .
Πρόσεξε τι γίνεται τώρα:
Γενικά, το δραστικό φορτίο πάει όπως σου είπα.
Υπάρχει όμως κι η εξής παράμετρος:
Για μια υποστιβάδα (ή στιβάδα αν μιλάμε για την s), ισχύουν τα εξής:
1)Άτομα με συμπληρωμένη την s ως εξώτατη, είναι περισσότερο σταθερά από άτομα με ημισυμπληρωμένη την s. Ηλεκτρόνια δε, σε μια συμπληρωμένη υποστιβάδα, είναι πιο σταθερά, από αυτά μιας μη συμπληρωμένης. Για αυτό και θα πρέπει να προσπαθήσεις ακόμη παραπάνω να πάρεις το δεύτερο ηλεκτρόνιο ns ενός ατόμου, από το πρώτο np, ακόμη κι αν αυτό τα καθιστά εξαίρεση στον κανόνα. (του κανόνα το ότι το δεύτερο έχει πιο πολλά πρωτόνια στον πυρήνα)
2)Όσον αφορά στις υποστιβάδες p και d, αυτό ισχύει όχι μόνο όταν είναι συμπληρωμένες, αλλά σε μικρότερο βαθμό, κι όταν είναι και ημισυμπληρωμένες (όταν έχει δηλαδή η p 3 και η d 5 ηλεκτρόνια). "Βολεύονται" με αυτή τη συμμετρία, και δεν τρελαίνονται να την χάσουν. (Για αυτό το λόγο άλλωστε, θα μάθατε και πως η δομή 4s23d4 γίνεται πιο σταθερή μόλις γίνει, 4s13d5. )
O κανόνας ο γενικός είναι αυτός που σου είπα πρίν. Όμως με αυτες τις δικαιολογημένες εξαιρέσεις, αντί να υπάρχει μια γραμμική σχέση περιοδικού πίνακα - ενέργειας ιοντισμού, υπάρχει η εξής.... σκάλα:

Βλέπεις που είναι το Mg και που το Al?
Καταλαβαίνεις ότι αυτό συμβαίνει λόγω του 1 που σου έγραψα;
Βλέπεις όμως επίσης, πως γενικά όσο πας δεξιά στον Π.Π, η τάση είναι ανοδική;
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Παιδιά το στοιχείο 12Mg έχει ηλεκτρονιακή δομή 1s2 2s2 2p6 3s2. θεωρούμε ότι έχει πολύ μεγάλη ενέργεια πρώτου ιοντισμού γιατί έχει δομή ευγενούς αερίου του ηλίου;
Δομή ευγενούς αερίου; Αυτό προκύπτει πως;
ΠΟΛΥ ΣΗΜΑΝΤΙΚΟ:
Για να μιλάμε για δομή ευγενούς αερίου, πρέπει να μιλάμε για συμπληρωμένη στιβάδα. Ολόκληρη. Ένα τροχιακό μόνο του δε λέει κάτι. Το ότι το He τυγχάνει και είναι το μόνο ευγενές αέριο με 2 e- στην εξώτατη, συμβαίνει ακριβώς επειδή η εξώτατή του τυγχάνει να είναι και η πρώτη στιβάδα, η οποία αποτελείται από ένα μόνο τροχιακό, κι άρα η οποία με 2 e- γεμίζει.
Οποιοδήποτε άλλο άτομο, για να είναι ευγενές, πρέπει να έχει και p υποστιβάδα συμπληρωμένη.
Κάνω αυτήν την παρένθεση, γιατί είναι πολύ σημαντικό αυτό ακόμη και ως διατύπωση. Μη μου συνδέσεις αλκαλική γαία που είναι πολύ δραστική με ευγενές αέριο, αλκαλική γαία θα δεις να κάνει άλατα, οξείδια, αντιδραστήρια Grignard, ο,τι μπορείς να φανταστείς.
Στην ερώτησή σου τώρα.
Υπονοείς πως επειδή το Mg, (σε σχέση με το Na προφανώς) έχει το 3s συμπληρωμένο, αποκτούν μια κάποια σταθερότητα εντός του τροχιακού αυτού αυτά τα e- που έχει αυτό, σε σχέση με το μονήρες 3s e- του Νa.
Ναι ισχύει, ωστόσο ο κυριότερος λόγος που η ενέργεια ιοντισμού του Mg είναι μεγαλύτερη (που πρέπει να δώσεις περισσότερη ενέργεια για να πάρεις ένα e- από το Mg με πιο απλά λόγια), είναι πως το Mg βάσει ατομικού αριθμού, εκτός από ένα περισσότερο ηλεκτρόνιο, έχει κι ένα περισσότερο πρωτόνιο στον πυρήνα του.
Μας νοιάζει;
Φυσικά. Γιατί; Γιατί αυξάνεται το δραστικό πυρηνικό φορτίο του.
Τι είναι το δραστικό πυρηνικό φορτίο;
Το φορτίο που "νιώθει" να δέχεται ένα εξωτερικό e- ενός ατόμου από τον πυρήνα, μετά από αφαίρεση των απώσεων από τα ενδιάμεσα e-

Στο δικό σου παράδειγμα, αυξάνεις το πυρηνικό φορτίο κατά +1.
Άρα, το εξωτερικό e- θα έλκεται κάπως περισσότερο.
Άρα, θα χρειάζεται μεγαλύτερη ενέργεια για ιοντισμό.
Γενικά:

Καλύπτεσαι;
Κατ'αρχας,μιλαμε για ενεργεια πρωτου ιοντισμου(επειδη βλεπω οτι το γραφεις σκετο ενερ.ιον.).Κατα δευτερον,δεν ειναι αναγκη να μιλας για πυρηνικα φορτια κλπ.Αν κανεις τις δομες,βρεις περιοδο και ομαδα και μιλησεις για το πως αυξανεται η ενεργεια πρωτου ιοντισμου,εισαι ok.Τα υπολοιπα ειναι σαλτσες για να περναει η ωρα και οχι απολυτως απαραιτητες.
Καλη συνεχεια!!
Και κάπως έτσι, έχουμε το ελληνικό σύστημα.

Σου απάντησα πάντως, επειδή ρώτησες το γιατί.
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


ναι, αυτη ακριβως ηταν και η ερωτηση που τεθηκε στην άσκηση. δεν παρέλειψα κάτι και εμένα μου φάνηκε ατελής η ερώτηση
https://en.wikipedia.org/wiki/Bromine_test
Το διάλυμα Βρωμίου έχει ένα χρώμα τέτοιο:

Εάν το δεις να εξαφανίζεται, σημαίνει πως είχες μέσα ακόρεστη ένωση, η οποία αντέδρασε με το μοριακό βρώμιο (σπάσιμο διπλού δεσμού, προσθήκη ατόμων βρωμίου)
Είναι κλασικό τεστ ύπαρξης ακόρεστης ένωσης (πχ αλκένιο) αυτό.
Δεν ξέρω αν αυτή ήταν η απορία σου.
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


παιδιά στην οργανική χημεία πως μπορούμε να διαπιστώσουμε αν έχει πραγματοποιηθεί μια αντίδραση προσθήκης;
Γίνε σαφής.
Ένα τυχαίο παράδειγμα που μου έρχεται στο μυαλο ειναι αποχρωματισμός Βρωμίου.
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Καλύτερος από τον Σαλτερή;
Σε πρώτο/δεύτερο δεν τίθεται σύγκριση καν,διαφορετικές κατηγορίες.Και όλη η ύλη σε ένα τόμο ε;
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Εχω αρχισει και αγχωνομαι ...Εγω καλα - καλα δεν εχω ξεκινησει φροντ και υπαρχουν τοσα παιδια π κανετε καλοκαιρινα...
Κούλαρε βρε θα βγάλεις την ύλη 2-3 φορές τουλάαααχιστον

Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Γιατι ο τρίτος άνθρακας ως τετράεδρο,θα κάνει τους τρεις δεσμούς του όχι στην ιδια ευθεία,αλλά ο δεσμός με τον δευτερο άνθρακα θα είναι ανάμεσα στο δεσμό με τον τέταρτο άνθρακα και το δεσμο με το Η (μιλάω για γωνίες)ΔΕΣ τις εικόνες και το συνημμένο,κάνε μια προσπάθεια.γτ ομως δεν μπορουμε να βαλουμε το διπλο δεσμο οκ σε ενα επιπεδο..μετα και τον αλλο ανθρακα με τα υδρογονα στο ιδιο επιπεδο..μεχρι εδω ετσι ειναι νομιζω(ισχυει δηλαδη αυτο)..και μετα γτ δν βαζουμε και τον αλλο ανθρακα στο ιδιο επιπεδο με τους αλλους 3? δηλαδη ο απλος δεσμος που θα γινει μεταξυ του 3 και 4 ανθρακα να γινει αφου βγαλουμε το H ΠΟΥ βρισκεται στο ιδιο επιπεδο με τους αλλους?

Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


ok ευχαριστω..απλα σε ρωτησα αν καποιο τουλαχιστον απο τα υδρογονα ειναι στο ιδιο επιπεδο με τον C...oxi αν ολα τα υγρογονα ειναι στο ιδιο επιπεδο
Φυσικά με δυο από αυτά είναι.Αφού 3 σημεία ορίζουν ένα επίπεδο.Για να σου λυθεί η απορία πήγαινε στο 5) του αρχειου που σου έδωσα,δες τις δομές,κι άλλαξε το ένα Η με CH3
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Για να σου πω την αλήθεια,τόση ώρα σου λέω κατά κάποιο τρόπο βλακείες.Η απορία σου εξηγείται απλά,αλλά είναι εκτός ύλης λυκείου.Δες:
https://www.biology.uoc.gr/courses/BIO6_Organiki_Ximia/Lectures/Lecture%204.pdf
Για το βουτάνιο,απλά αντικατέστησε ένα από τα Η με CH3.Για να καταλάβεις το σχήμα,φαντάσου πως βλέπεις την ένωση από μπροστά(όχι από τα πλάγια),κι ότι ο κύκλος είναι ο δεσμός που περιστρέφεις.Το όλο θέμα είναι ενεργειακό.
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


εμας μας ειπε κατι οτι επειδη στο 1 βουτενιο 2 τετραεδρα δν γινεται να εχουν το ιδιο κεντρο στο ιδιο επιπεδο μπορεις να το εξηγησεις? μου χρειαζεται να ξερω αν βρισκονται στο ιδιο επιπεδο? εμεις κανουμε για τα υβριδικα τροχιακα αλλα δν ειδα να λεει κατι τετοιο
Ακριβώς το ίδιο λέμε.Στο 1- βουτένιο,δυο συνεχόμενοι άνθρακες είναι μόνο με απλούς δεσμόυς(υβριδισμός sp3,4υποκαταστάτες),άρα είναι τετράεδρα.Τετράεδρο και τετράεδρο που ενώνονται και με άλλους ανθρακες δεν έιναι στο ίδιο επίπεδο με εκείνους.Πάρε τον τρίτο ανθρακα από αριστερά (ξαναλέω) στο 1-βουτένιο ως κεντρικό,και σύγκρινε τον με αυτό του μεθανιου.Διαφέρουν στο ότι ο ένας έχει υδρογόνα ως υποκαταστάτες ενώ ο άλλος άνθρακες.Στο βουτένιο,οι υπόλοιποι άνθρακες (αυτοί οι δυο με το διπλό,λειτουργούν ως υποκαταστάτες πλέον του τρίτου άνθρακα.Σου είπα να αντικαταστήσεις τα δυο υδρογόνα στην περιπτωση του μεθανίου με μεθύλιο και με την άλλη ομάδα,για να καταλάβεις την ομοιότητα.Τα υδρογόνα του μεθανίου είναι στο ίδιο επίπεδο;Οι υποκαταστάτες του τρίτου άνθρακα στο ένα βουτένιο τότε γιατί να είναι,αφού κι αυτός,και κάθε άνθρακας που κάνει 4 δεσμούς,τους στρέφει προς τις ίδιες κατευθύνσεις.)
Οι εικόνες δε βοήθησαν να αποκτήσεις μια άποψη;
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


ερωτηση:πως αιτιολογω οτι στο 1 βουτενιο δεν βρισκονται ολη οι ανθρακες στο ιδιο επιπεδο??? θελω μια αναλυτικη εξηγηση ετσι ωστε να το καταλαβω...
ενω στο 2 βουτενιο ολοι βρισκονται στο ιδιο επιπεδο???

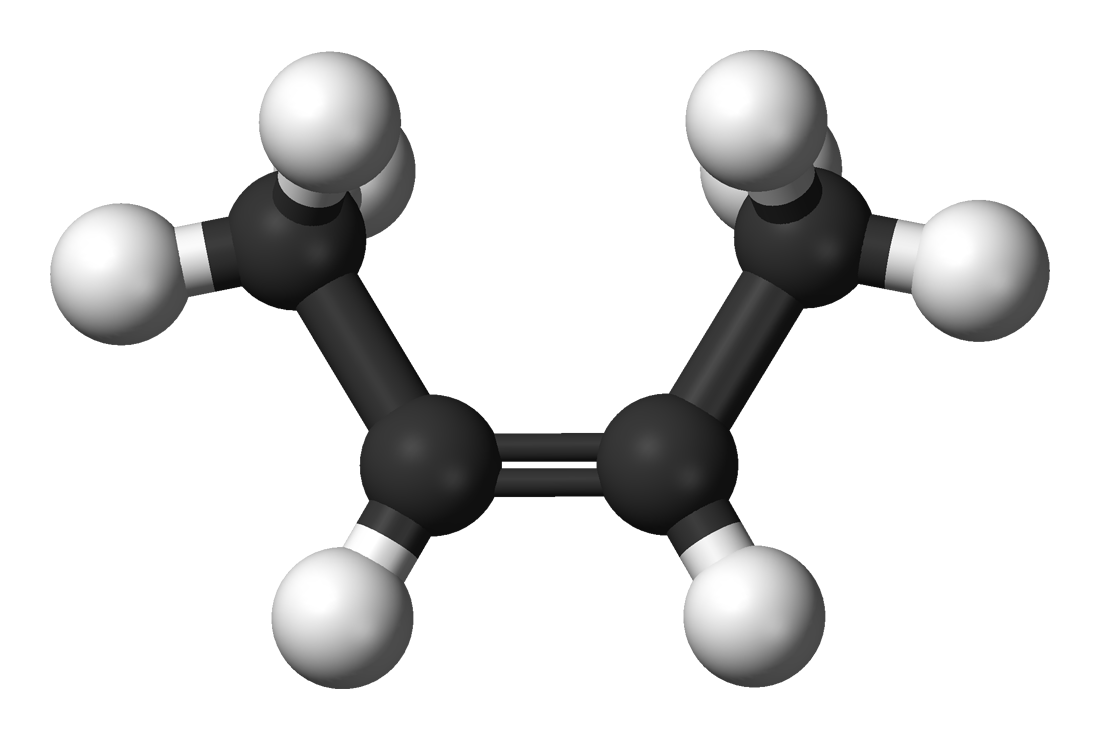
Δυο άνθρακες με διπλό δεσμό είναι στο ίδιο επίπεδο.Όταν τρεις άνθρακες ενώνονται διαδοχικά με δυο απλούς δεσμούς έχουμε δυο επίπεδα.Γενικά κάθε άνθρακας που έχει απλούς μόνο δεσμούς,όπως ο επόμενος άνθρακας στο 1-βουτένιο από αυτόν που έχει το διπλό(δηλαδή ο τρίτος από αριστερά,έχει δομή τετράεδρου,όπως και η απλή περίπτωση του μεθανίου.
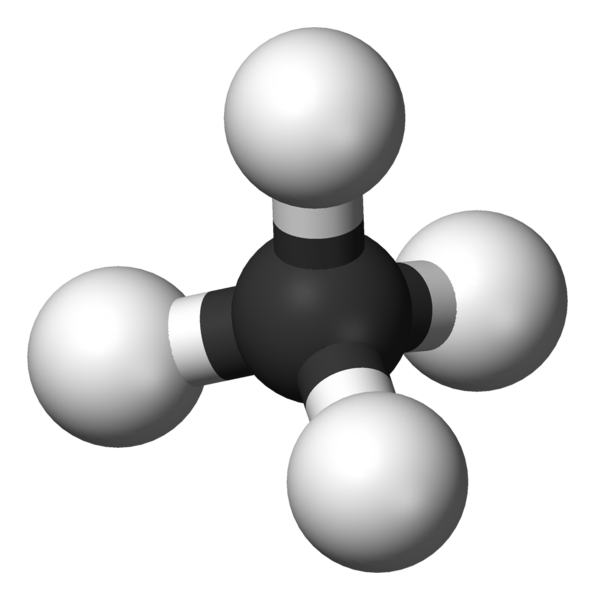

Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Δηλαδή, πρέπει να ξέρουμε ότι κατά μήκος της περιόδου αυξάνεται ο ομοιοπολικός χαρακτήρας.
Κάτι τέτοιο έχε στο νου σου και μέσα σε μια ομάδα από πάνω προς τα κάτω,αλλά αντίστροφα,στην περίπτωση της ομάδας 13 βλέπεις πχ:Αύξηση μεγέθους,μείωση ηλεκτραρνητικότητας κι ακόμα κι αν το πάνω είναι αμμέταλο,κάτω έχεις μέταλλα.
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος



Προφανώς λάθος.

Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Ερωτήσεις τύπου "πρέπει να τα ξέρω;",δεν μπορούν να απαντηθούν από εμένα,δυστυχώς.Όχι τίποτα,δε θυμάμαι και θα σε κάψω κιόλας.Ό,τι μαθαίνουμε καλό είναι.
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Το Η κάνει ιοντικούς δεσμούς στα υδρίδια μετάλλων, πχ CaH₂, με αριθμό οξείδωσης -1 !
Με κάλυψε ο Δίας,γι'αυτό είπα "είναι ιοντικός ο δεσμός HCl;"αντί να πω "κάνει το Η ιοντικούς δεσμούς;"

Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Η άσκηση λέει ότι ο δεσμός του υδροχλωρίου είναι ιοντικός,ή πρέπει να πάω να ρίξω νερό στο πρόσωπο μου;

Μήπως οι περίοδοι είναι 2η,3η και 4η;


To H είναι ΑΜΕΤΑΛΛΟ.Ο Δίας δεν έχει εργαστεί λάθος.Η η ίδια η ερώτηση είναι λάθος,ή ξυπνήστε με .
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Ηράκλειο.Θα αρχίσω το τρίτο.Σε ποια πολη σπουδαζεις και σε ποιο ετος;;;
σε ευχαριστω πολυ..οι διακεκομενες γραμμες τι ειναι? και τι σημαινει σ-δεσμος?
Τι τάξη είσαι;Για να ξέρω κατά πόσο θα μπω εκεί.
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Για την ακρίβεια φοιτητής χημικού.Χημικος είσαι;;;
τελεια! Αυτο αυτο ακριβως θελω να γινω και εγω!
Λατρευω την χημεια
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Το εξηγησες παααρα πολυ καλα! Μπραβο σου!
Όταν θα γίνουμε συνάδελφοι θα κάνεις το ίδιο.

Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος



H παύλα στο άζωτο θα μπορούσε να συμβολιστεί με δυο τελείες.Δυο ηλεκτρόνια.Η διαφορά αυτού του δεσμού με τον ομοιοπολικό,είναι οτι εδώ το ένα άτομο προσφέρει και τα δυο ηλεκτρόνια για το μοίρασμα.(Ενώ ο ιοντικός σημαίνει κλέβω ενα ηλεκτρόνιο από κάποιον και το έχω μόνο για μένα)
Τα αλογόνα κάνουν μόνο ένα δεσμό,γιατί στην εξωτερική τους στιβάδα έχουν 7 ηλεκτρόνια,τρια ζευγάρια κι ένα μόνο του.Το μόνο του θα συζευκτεί με ένα άλλο ηλεκτρόνιο άλλου ατόμου,ώστε να γίνουν τα ηλεκτρόνια οκτάδα,κι έτσι θα υπάρξει ένας δεσμός.
Σημείωση: Το μήνυμα αυτό γράφτηκε 12 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


nNaOH = m/Mr = 0,4 / 40 = 0,01 mol
C NaOH = nNaOH / VNaOH = 0,01 / 0,1L = 0,1 M
C OH- = CNaOH επειδή ιοντίονται ΟΛΑ τα μορια του ΝαΟΗ σε Να+ + ΟΗ-
Άρα C OH- = 0,1 M = 10 εις την -1
Κw = C OH- X C H3O+ = 10 στην πλην 14 ===>
10 εις την -1 Χ CH3O+ = 10 εις την πλην 14 ===>
CH3O+ = Kw/C OH = 10 εις την πλην 13
pH = -logCH3O+ = -log10 εις την πλην 13 = 13

Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Γιατι υδατικο διαλυμα CCl3COOH εχει μικροτερη τιμη pH απο υδατικο διαλυμα CH3CH2COOH ιδιας συγκεντρωσης και στην ιδια θερμοκρασια??
Για δυο λόγους.Κατ'αρχην το Cl σε σχέση με το Η,έχει μεγαλύτερη ηλεκτραρνητικότητα,που σημαίνει πως τραβά τα κοινά ηλεκτρόνια τον δεσμών περισσότερο προς το μέρος του,κι άρα μετακινεί προς τον εαυτό του περισσότερο τ ηλεκτρονιακό νέφος,κι έτσι το Η+ αποσπάται ευκολότερα.Επίσης,το CH3CH2CH2CH2CH2COOH για παράδειγμα θα είναι λιγότερο όξινο από το CH3COOH,επειδή όσο μεγαλύτερη η αλυσίδα (όταν δεν έχεις υποκαταστάτες εκτός Η),τόσο πιο πολλά ηλεκτρόνια υπάρχουν να προσφερθούν επαγωγικά,(φαινόμενο αντίθετο με αυτό που προκαλεί το Cl),κι επειδή το νέφος μετατοπίζεται προς το όξινο Η+, αυτό αποσπάται δυσκολότερα.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Μα, αυτό δεν έλεγε και ο φίλος στην εκφώνηση? (κατάλαβα λάθος?). Αν έχεις χρόνο και όρεξη, δες σε παρακαλώ και αυτό που ρώτησα παραπάνω.
Πολύ ενδιαφέρον (και το site επίσης), σ΄ευχαριστώ. (Μάλλον υπερβολικό για πανελλήνιες ε?).
Καλή χρονιά ξανά...

Υπερβόλικότατο,αλλά καλώς το ψάχνεις.Καθηγητής Φυσικής πρέπει να ξέρει και Χημεία.
Οσο για την ένωση,το παιδί έλεγε RNH2Cl,2 αντι 3,μου τρώει έναν υποκαταστάτη.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Ποιο είναι το λάθος? Δεν στέκουν οι αντιδράσεις:
RNH₃Cl → RNH₃⁺ +Clˉ και RNH₃⁺ +H₂0 ⇄ RNH₂+H₃O⁺ ?
ή μάλλον δεν υπάρχει το RNH₃Cl ? (ίσως είναι ποιητική άδεια).
Μόνος σου είπες πως το σωστό είναι RNH3Cl
Μια που δε βρήκα έχω μια άλλη απορία:
Σε μια άσκηση του σχολικού (19α σελ.143) δίνει την αντίδραση:
2H₂SO₄ + HNO₃ → H₃O⁺ + NO₂⁺ + 2HSO₄ˉ
και ρωτάει ποια ουσία κατά την κατεύθυνση του βέλους δρα ως οξύ και ποια είναι η συζυγής βάση της. Ωραία, απαντάμε H₂SO₄ και HSO₄ˉ. Αλλά το άλλο ζευγάρι οξύ/βάση ποιο είναι? (Δεν την είχα προσέξει όταν την έκανα, τώρα με την επανάληψη μου χτύπησε στο μάτι).
Καλή χρονιά...

To HNO3 είναι ασθενέστερο οξύ,οπότε έχεις στιγμιαία το προιόν [H2NO3] το οποιο διασπάται σε NO2+ ΚΑΙ Η2Ο
Συζήτηση σχετικά
Οπότε η άλλη βάση είναι το HNO3,με συζηγές οξυ αυτο που διασπάται.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Εγώ δεν έχω Σαλτερή καν.Δεν δοκίμασα να τη λύσω.Btw επιμένω πως το RNH2 μαλλον δεν ειναι σωστό.Sorry, κάτι δεν μου πάει καλά με αυτή την άσκηση. Δίνει Κα = 10⁻⁹. Όμως για C=1M και pH=5 βγάζω Κα = 10 ⁻ˈ⁰ . Με το 10⁻⁹ δεν λύνεται η άσκηση (βγάζει για το τελικό C=0,01Μ), με το 10 ⁻ˈ⁰ λύνεται. (Έχω το Σαλτερή, αλλά δεν την βρήκα).
Καλή χρονιά...

Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Είναι RNH₃Cl και στις δύο περιπτώσεις.Επειδή δεν κατάλαβα τι έγραψες,γράφω τις αντιδράσεις για να δεις πως το σκέφτομαι.
RNH₃Cl→RNH₃* +Cl-
RNH₃*+H₂0⇔RNH₂+H₃O* Αφού προσθέτουμε RNH₃Cl,στην ουσία δεν αυξάνουμε τα κατιόντα RNH₃* ; Γιατί λέει ότι το pH αυξάνεται;
Αγόρι μου το pH είναι με πολύ απλά λόγια το ποσοστό της ουσιας στο νερό.(Με πολυ απλά λογια)Αν αυξάνεις την ουσία,αλλά αυξάνεις το νερό ακόμα περισσότερο,τότε τι κανεις?
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Δεν έχω scanner και αν την βγάλω φωτογραφία,θα βγει τεράστια και δεν θα φαίνεται καλά.Τι θέλεις να δεις,να στο πω εγώ;
Δες το ποστ μου μετά τις επεξεργασίες.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Ακριβώς.Ο Pauli λεει:ΑΠΑΓΟΡΕΥΕΤΑΙ σε ενα ατομο,δυο ηλεκτρόνια να εχουν 4 κβαντικους αριθμους ισους.Είπα λαλακία... Τα μονήρη είναι που αφορούν τον Hund.
Δηλαδή αν εχουν τους τρείς(στιβαδα-υποστιβάδαm-τροχιακό,ο ms που καθοριζει το spin θα ειναι de facto διαφορετικος.)
Αυτο εξυπακουεται οτι ενα τροχιακο χωραει το πολύ δυο ηλεκτρονια (υπαρχουν δυο δυνατοι ms +/- 1/2)
Ο Pauli ρησιμοποιείται ΣΥΝΗΘΩΣ (οχι παντα) σε περιπτωσεις ηλεκτρονιων ιδιου τροχιακού.Αν δηλαδη δεις κάτι της μορφής (^^)-σκεψου το σαν βελακια-παραβιαζεται ο pauli.
O Ηund αφορα εναν ευρύτερο αριθμό ηλεκτρονίων,σε στοιβαδες με περισσοτερα των 1 τροχιακών,κοινως εκτος της s. στη στιβαδα p πχ,αν δεις κατι της μορφης (^)(^)(ν) παραβιαζεται ο Ηund,του οποιου ή αρχη λέει:Σε υμισυμπληρωμενες στιβαδες,τα ηλεκτρονια διατασσονται στα τροχιακα αυτών,ετσι ωστε να έχουν τη μεγιστη απολυτη τιμη αθροίσματος spin.(δηλαδη αν εχεις 3 ηλεκτρονια πχ στην p ή 3/2 ή -3/2,ενώ δυο e- με αντιθετο spin μας δινουν 0 στο σύνολο,οποτε τοτε προκυπτει 1/2 και απορριπτεται.)
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Ευχαριστω που ασχοληθηκες φιλε, αλλα καπου κανεις λαθος. Στη λυση βγαινει V1:V2 = 3:10. Γραφει επισης (στη λυση) οτι η αντιδραση που πραγματοποιειται ειναι: HA + OH- --> A- + H3O+. Μετα λεει, ειναι n(HA) = 0,5V1 mol και n(OH-) = 0,1V2 mol. Και τελικα V1:V2 = 3:10
Προσωπικα δε βγαζω νοημα απο τη λυση. Αυτη η ασκηση ειναι στο βοηθημα του Σαββαλα ακριβως πριν το κεφαλαιο των ρυθμιστικων, στην εκδοση μου η τελευταια.
βασικα V1 και V2 για αυτον ειναι ο,το το χ και ψ για μενα δεν κολλαμε εκει...το 0,1 ειναι ειπαμε επειδη η βάση ειναι ισχρη με ρΗ 13 απο κει και περα ομως πως δουλευει...?αντιδρα η βαση του στο διαλυμα της πριν τα αναμιξει η εχει το νερο και τα προσθετει...?κι εστω οτι αντιδρα πρωτα η βαση που εγω εβαλα Β- και διισταται πληρως σε ΟΗ- αφου ειναι ισχυρη...το ΗΑ αφου ειναι ασθενες μασ δινει το δικαιωμα να πιστευουμε πως και ι Α- μπορει να αντιδρα με το νερο,αυτο δεν καταλαβαινω.ασ πουμε δηλαδη πως η ισχυρη βαση ειναι ΝαΟΗ,γινεται ολη ΟΗ- και το ασθενες οξυ τυχαια λεω CH3COOH tote kai η A- dld i CH3COO- θα αντιδρα...και παλι επρεπε να βγαινει κανε το πινακακι που εκανα και στην αντιδραση αφαιρεσe τα 0,1V2 mole.Το οξυ ειναι σε περισσεια γιατι εχεισ οξινο ρΗ με ισχυρη βαση.μετα παρε CH3O+=riza KaXcοξεος το Cοξεος ομως ισουται με το C bashs που εφυγε,εχεις και την Κα του HA,kai ti Coksonion apo to pH = 4 ti sto kalo ola ta heis ?
 tha tin psakso otan vro hrono sou to iposxomai.
tha tin psakso otan vro hrono sou to iposxomai.Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Ευχαριστω!!
Καμια ιδεα για αυτη την ασκηση υπαρχει? Υδατικο διαλυμα ασθενους οξεος ΗΑ 0,5Μ εχει pH = 2 (Δ1), ενω υδατικο διαλυμα ισχυρης βασης εχει pH = 13 (Δ2). Να υπολογισετε με ποια αναλογια ογκων πρεπει να αναμιξουμε τα διαλυματα Δ1 και Δ2, ωστε να προκυψει διαλυμα Δ3 με pH = 4. Ολα τα διαλυματα εχουν θερμοκρασια 25°C.
Υπολογισα Κα(ΗΑ) = 2*10^-4.
ανεβάζω ενα συνημενο δεν ξερω...φαίνεται?
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Chemwizard
Τιμώμενο Μέλος


Θα σε γελάσω και δεν το θέλωΘα ρωτήσω το χημικό μου και αν έχει κάτι κατά νου θα το ποστάρω..!

Σας παραθ'ετω τι λέει η Γενική Χημεία Ebbing/Gammon:
Εφόσον σχηματίζει τον αιθανικό ισοπροπυλεστέρα, το αλκυλοχλωρίδιο είναι το 2-χλωροπροπάνιο. Άρα έχει συντακτικό τύπο CH3CHClCH3. Τώρα αντίδραση με Ag δεν θυμάμαι κάποια. Μπορεί βέβαια να μου διαφεύγει αυτή την στιγμή...
To AgCl (σε νερο κι οχι αμμωνια)ειναι δυσδιαλυτο.Πραγμα που έχω πει πως ευνοεί αντιδρασεις με αυτο το προιόν.οπότε προσανατολήσου προς τα εκει.την αντιδραση δεν την εχω κανει,αλλα 2-χλωρο-προπανιο να αντιδρα με Ag2O...χμ...μου μυριζει 2-xloropropanio(dio tetoia)+Ag20--->2διμεθυλεστερας(X2)+2AgCl+H2O ??? (λογικό ακούγεται)
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
-
Το forum μας χρησιμοποιεί cookies για να βελτιστοποιήσει την εμπειρία σας.
Συνεχίζοντας την περιήγησή σας, συναινείτε στη χρήση cookies στον περιηγητή σας.
 Αρχική Forum
Αρχική Forum
 Ρωτήστε κάτι
Ρωτήστε κάτι
 Προσωπικές Συζητήσεις
Προσωπικές Συζητήσεις
 Πανελλαδικές
Πανελλαδικές
 Αγγελίες
Αγγελίες
 Συνδεδεμένοι Χρήστες
Συνδεδεμένοι Χρήστες
 Λίστα Αποκλεισμένων
Λίστα Αποκλεισμένων
 Υπεύθυνοι του Forum
Υπεύθυνοι του Forum
 e-steki
e-steki