
26-08-10

19:52
α)Έχεις 1s2 2s2 2p6 3s2 3p6 (μετά τα 3p τροχιακά συμπληρώνονται τα 4s) 4s1. Άρα ο ελάχιστος ατομικός αριθμός είναι ο 19.
Το να βρεις το μέγιστο για κυριο κβαντικό αριθμό μεγαλύτερο του 3 είναι αρκετά πολύπλοκο και έξω από τα πλαίσια του λυκείου.
Εν πάσει περιπτώσει η δομή του τελευταίου στοιχείου που συμπληρώνει τροχιακό με κύριο κβ. αριθμό 4 είναι το στοιχείο με ατομικό αριθμό 70.
Για κ.κ.α.=4 έχουμε μέχρι και f τροχιακά.
Τα τροχιακά συμπληρώνονται με τη σειρά ως εξής (https://upload.wikimedia.org/wikipedia/commons/1/11/Electron_orbitals.svg):
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d κλπ.
Γενικώς ισχύει ότι η ενέργεια ενός τροχιακού είναι περίπου ανάλογη με το άθροισμα των κβ. αριθμών n και l με τον n να παίζει κάπως σημαντικότερο ρόλο.
Ακολουθώντας αυτόν τον κανόνα έχουμε ότι μέχρι και το 6s τα συμπληρώνουμε όλα (αφού εμείς θέλουμε να καλύψουμε ΚΑΙ όλα τα 4f).
Τα 4f και 5d έχουν n+l ίσο με 4+3=5+2=7, άρα τα τροχιακά έχουν περίπου την ίδια ενέργεια και συνεπώς είναι δύσκολο να ξέρουμε ποιο από τα δύο έχει μικρότερη ενέργεια με κάθε ηλεκτρόνιο που προσθέτουμε. Θα μπορούσαμε ωστόσο να σκεφτούμε ότι επειδή τα 4f έχουν μικρότερο n θα συμπληρώνονται πρώτα. Αυτό ΔΕΝ ισχύει πάντα μέχρι να συμπληρωθούν τα 4f, αλλά είναι ο κανόνας. Επίσης ξέρουμε ότι τα συμπληρωμένα και ημισυμπληρωμένα τροχιακά έχουν χαμηλότερη ενέργεια. Άρα μπορεί να μην ξέρουμε πως συμπλρώνονται άτομα με ενδιάμεσο ατομικό αριθμό, αλλά όταν συμπληρωθούν τα 4f δε θα έχουμε ούτε ένα e- στα 5d γιατί αν υπάρχει έστω ένα θα πάει στα 4f για την πλήρη συμπλήρωση (ή την ημισυμπλήρωση).
Δεν μπορώ να πω τίποτε άλλο χωρίς να ξεφύγω κατά πολύ από τα πλαίσια του λυκείου.
β) 1) ένα. (4s1 βλ. πάνω)
2) τα l=1 είναι τα p άρα 6.
3) Πρώτα θα φύγει το 1 από το 4s και μετά άλλο ένα από τα 3p. Άρα 1s2 2s2 2p6 3s2 3p5.
Το να βρεις το μέγιστο για κυριο κβαντικό αριθμό μεγαλύτερο του 3 είναι αρκετά πολύπλοκο και έξω από τα πλαίσια του λυκείου.
Εν πάσει περιπτώσει η δομή του τελευταίου στοιχείου που συμπληρώνει τροχιακό με κύριο κβ. αριθμό 4 είναι το στοιχείο με ατομικό αριθμό 70.
Για κ.κ.α.=4 έχουμε μέχρι και f τροχιακά.
Τα τροχιακά συμπληρώνονται με τη σειρά ως εξής (https://upload.wikimedia.org/wikipedia/commons/1/11/Electron_orbitals.svg):
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d κλπ.
Γενικώς ισχύει ότι η ενέργεια ενός τροχιακού είναι περίπου ανάλογη με το άθροισμα των κβ. αριθμών n και l με τον n να παίζει κάπως σημαντικότερο ρόλο.
Ακολουθώντας αυτόν τον κανόνα έχουμε ότι μέχρι και το 6s τα συμπληρώνουμε όλα (αφού εμείς θέλουμε να καλύψουμε ΚΑΙ όλα τα 4f).
Τα 4f και 5d έχουν n+l ίσο με 4+3=5+2=7, άρα τα τροχιακά έχουν περίπου την ίδια ενέργεια και συνεπώς είναι δύσκολο να ξέρουμε ποιο από τα δύο έχει μικρότερη ενέργεια με κάθε ηλεκτρόνιο που προσθέτουμε. Θα μπορούσαμε ωστόσο να σκεφτούμε ότι επειδή τα 4f έχουν μικρότερο n θα συμπληρώνονται πρώτα. Αυτό ΔΕΝ ισχύει πάντα μέχρι να συμπληρωθούν τα 4f, αλλά είναι ο κανόνας. Επίσης ξέρουμε ότι τα συμπληρωμένα και ημισυμπληρωμένα τροχιακά έχουν χαμηλότερη ενέργεια. Άρα μπορεί να μην ξέρουμε πως συμπλρώνονται άτομα με ενδιάμεσο ατομικό αριθμό, αλλά όταν συμπληρωθούν τα 4f δε θα έχουμε ούτε ένα e- στα 5d γιατί αν υπάρχει έστω ένα θα πάει στα 4f για την πλήρη συμπλήρωση (ή την ημισυμπλήρωση).
Δεν μπορώ να πω τίποτε άλλο χωρίς να ξεφύγω κατά πολύ από τα πλαίσια του λυκείου.
β) 1) ένα. (4s1 βλ. πάνω)
2) τα l=1 είναι τα p άρα 6.
3) Πρώτα θα φύγει το 1 από το 4s και μετά άλλο ένα από τα 3p. Άρα 1s2 2s2 2p6 3s2 3p5.
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

17-03-10

21:46
Το βοήθημα είναι σωστό. Ζητάει τον ελάχιστο ατομικό αριθμό.Παιδια μια απορια για να μην ανοιγω καινουριο θεμα. Στο βοηθημα εχει μια ασκηση, λεει να βρω τον ελαχιστο ατομικο αριθμο στοιχειου, το ατομο του οποιου στη θεμ. κατασταση εχει 5 ηλεκτρονια σε d τροχιακα. Εγω λεω οτι ειναι Z=25, στην απαντηση γραφει ομως 24. Ποιο ειναι το σωστο;
Τα ημισυμπληρωμένα d τροχιακά έχουν χαμηλότερη ενέργεια, άρα προτιμώνται και παρότι συμπληρώνεται πρώτο το 4s τροχιακό με δύο ηλεκτρόνια, αφού θα έχεις 4 στο 3d, θα μεταφέρεις το ένα ηλ. στο 3d. Οπότε, αν έχεις ένα άτομο στη θεμελιώδη κατάσταση με 24 ηλεκτρόνια, αυτά θα κατανεμηθούν ως εξής:
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

27-02-10

17:49
Μάλλον δε θα θέλεις ακόμα τη λύση, αλλά οκ...βοήθεια σε άσκηση στα ρυθμιστικά του ανοιχτού πανεπιστημίου:
α)να υπολογισθεί η σταθερά ιοντισμού ενός δείκτη Hln γνωρίζοντας ότι ο δείκτης αλλάζει χρώμα όταν έχει μετατραπεί κατα 1/8 στην ιοντική του μορφή και ότι η χρωματική αλλαγή γίνεται σε pH=8.3
β) θα μπορούσε ο παραπάνω δείκτης να χρησιμοποιηθεί στην ογκομέτρηση υδατικού διαλύματος CH3COOH 0.10M για τον ακριβή προσδιορισμό του ισοδύναμου σημείου;
a)Τη στιγμή που γίνεται η χρωματική αλλαγή:
και
b)Ναι θα μπορούσε. Το ισοδύναμο σημείο του, επειδή είναι ασθενές οξύ και άρα το άλας που θα παραχθεί κατά την εξουδετέρωση διίσταται μερικώς, είναι πάνω από το 7. Από ό,τι θυμάμαι κιόλας από πέρυσι από το εργαστήριο ανόργανης χημείας πράγματι το ισοδύναμο σημείο βρίκσεται κάπου γύρω το 8.5. Βέβαια, θα έπρεπε να σου δίνει και την σταθερά ισορροπίας του οξικού οξέος για να απαντήσεις πλήρως...
Αλήθεια τι σχέση έχει η άσκηση με τα ρυθμιστικά διαλύματα;
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

24-12-08

17:48
Μία σχετικά παρόμοια άσκηση για να εξασκηθείς:
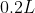
})
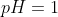 αναμιγνύονται με
αναμιγνύονται με 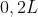
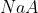
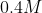 . Βρες το pH του τελικού δ/τος.
. Βρες το pH του τελικού δ/τος. 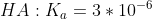
Υπόδειξη: 6 θα βρεις.
Υπόδειξη: 6 θα βρεις.
Σημείωση: Το μήνυμα αυτό γράφτηκε 15 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

23-12-08

16:42
Λοιπόν, θα σου δώσω σημαντικές υποδείξεις.
Το πρώτο ερώτημα το βρήκες σωστά btw...
β) 0,1Μ ισχυρού οξέος συνεπάγεται 0,1Μ H3O+.
Άρα τώρα θα πάρεις την ιοντική ισορροπία δεδομένου ότι αρχικά έχεις και μία συγκέντρωση H3O+ 0,1Μ.
γ) NaOH-> ισχυρή βάση => όμοια με β...
Το πρώτο ερώτημα το βρήκες σωστά btw...
β) 0,1Μ ισχυρού οξέος συνεπάγεται 0,1Μ H3O+.
Άρα τώρα θα πάρεις την ιοντική ισορροπία δεδομένου ότι αρχικά έχεις και μία συγκέντρωση H3O+ 0,1Μ.
γ) NaOH-> ισχυρή βάση => όμοια με β...
Σημείωση: Το μήνυμα αυτό γράφτηκε 15 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

20-07-08

14:33
Το ΔΠΦ (δραστικό πυρηνικό φορτίο) ισούται το φορτίο του πυρήνα πλην τα ηλεκτρόνια των εσωτερικών στιβάδων. Άρα έλαβα υπόψη μου και τα ηλεκτρόνια των εσωτερικών στιβάδων.Και τα ενδιάμεσα ηλεκτρόνια είναι καλό να αναφέρει και ας μην το αναλύσει παραπάνω.
Βέβαια με τους άσχετους τους διορθωτές των πανελληνίων καλό θα ήταν να το αναφέρεις τώρα που το σκέφτομαι...
Σημείωση: Το μήνυμα αυτό γράφτηκε 16 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

16-07-08

14:05
Μία ολοκληρωμένη απάντηση
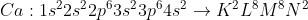
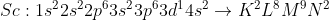
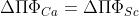 και τα δύο στοιχεία είναι στην ίδια περίοδο.
και τα δύο στοιχεία είναι στην ίδια περίοδο.
Όμως: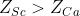 , άρα
, άρα 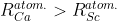 .
.
Η ενέργεια πρώτου ιοντισμού εξαρτάται από την ατομική ακτίνα (μεγαλύτερη ατομική ακτίνα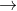 μικρότερη πρώτη ενέργεια ιοντισμού) και το ΔΠΦ. Αφού το δραστικό πυρηνικό φορτίο είναι ίδιο και για τα δύο άτομά μας όμως η ατομική ακτίνα του Sc είναι μεγαλύτερη η ενέργεια πρώτου ιοντισμού είναι μεγαλύτερη για το στοιχείο Sc.
μικρότερη πρώτη ενέργεια ιοντισμού) και το ΔΠΦ. Αφού το δραστικό πυρηνικό φορτίο είναι ίδιο και για τα δύο άτομά μας όμως η ατομική ακτίνα του Sc είναι μεγαλύτερη η ενέργεια πρώτου ιοντισμού είναι μεγαλύτερη για το στοιχείο Sc.
Σημείωση: Τις λέξεις με τα έντονα πλάγια γράμματα κατά λάθος τις παρέλειψα και τις πρόσθεσα τώρα.
Όμως:
Η ενέργεια πρώτου ιοντισμού εξαρτάται από την ατομική ακτίνα (μεγαλύτερη ατομική ακτίνα
Σημείωση: Τις λέξεις με τα έντονα πλάγια γράμματα κατά λάθος τις παρέλειψα και τις πρόσθεσα τώρα.
Σημείωση: Το μήνυμα αυτό γράφτηκε 16 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
-
Το forum μας χρησιμοποιεί cookies για να βελτιστοποιήσει την εμπειρία σας.
Συνεχίζοντας την περιήγησή σας, συναινείτε στη χρήση cookies στον περιηγητή σας.
 Αρχική Forum
Αρχική Forum
 Ρωτήστε κάτι
Ρωτήστε κάτι
 Προσωπικές Συζητήσεις
Προσωπικές Συζητήσεις
 Πανελλαδικές
Πανελλαδικές
 Αγγελίες
Αγγελίες
 Συνδεδεμένοι Χρήστες
Συνδεδεμένοι Χρήστες
 Λίστα Αποκλεισμένων
Λίστα Αποκλεισμένων
 Υπεύθυνοι του Forum
Υπεύθυνοι του Forum
 e-steki
e-steki