Αέριο μείγμα

έχει μάζα 10g. Δίνεται
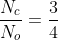
. Να βρείτε:

, τον όγκος του μίγματος, η % w/w και % v/v σύσταση του μίγματος.
Wow, πολύ νέκρα έχει πέσει εδώ, ας εγκαινιάσω το topic

Λοιπόν, έχουν περάσει πόσα χρόνια από τότε που διατυπώθηκε η εν λόγω άσκηση αλλά ας την λύσω...
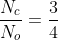
<=>
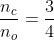
<=> n_c = 3/4 n_o <=>

<=>
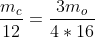
<=>
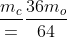
<=>
m_c = o,5625 m_o (βρήκαμε έτσι την σχέση των μαζών των ατόμων των 2 στοιχείων)...
m_c + m_o = 10 <=> o,5625m_o + m_o = 10 <=> 1,5625 m_o =10 <=> m_o = 6,4 gr και άρα m_c = 3,6 gr => n_o= m_o/ Ar_o = 6,4 / 16 = 0,4 mol και n_c= m_c / Ar_c = 3,6 / 12 =0,3 mol
Ξέρουμε ότι : n_co= n_c1 / δ = x/1= x mol και ομοίως n_co2= n_c2/ δ= y/1= y mol
m_co + m_co2= 10 =>
28x + 44y= 10 (σχέση 1) και ακόμη έχουμε την σχέση
x+y= 0,3(σχέση 2) , οπότε λύνοντας το σύστημα των δύο εξισώσεων με αντίθετους συντελεστές βρίσκουμε ότι x= 0,2 mol και y= 0,1 mol άρα m_co2 = n * Mr= 0,1 * 44 gr= 4,4 gr και m_co = n* Mr= 0,2 * 28 gr= 5,6 gr
Tώρα για τις περιεκτικότητες % w/w: Σε 10 gr μείγματος --> 4,4 gr co2
Σε 100 gr μείγματος --> 44 gr co2 (44% w/w)
Σε 10gr μείγματος--> 5,6 gr co
Σε 100 gr μείγματος--> 56 gr co (56 % w/w)
To ερώτημα για τους όγκους είναι λίγο πολύ λανθασμένο γιατί θα επρεπε να ξέρουμε και τις συνθήκες P, T στις οποίες βρίσκονται τα αέρια

Αν πχ βρίσκονται σε STP (Τ= 273,16 Κ και Ρ= 101325 Pascal) τότε: Vco= n * Vm = 0,2 * 22,4 L 4,48 L και Vco2= n* Vm= 0,1 * 22,4L = 2,24 L => Vολικό= V1 + V2= 6,72 L οπότε προκύπτει ότι έχουμε 66,7%v/v σε co και 33,3% ν/ν σε co2
N_o = n_o * NA = 0,4 NA άτομα Ο(τέλος)
Ας βάλω μία δική μου και ας ελπίσουμε να υπάρξουν ενδιαφερόμενοι...
Έχουμε 15 gr δείγματος ψευδαργυρου (ακάθαρτος ψευδάργυρος) τα οποία αντιδρούν με περίσσεια HCl οπότε κατά την αντίδραση εκλύονται 4,48 L αερίου σε STP συνθήκες. Να υπολογίσετε την περιεκτικότητα σε καθαρό ψευδάργυρο που έχει το εν λόγω δείγμα! (οι προσμείξεις του δείγματος θεωρούνται αδρανείς)...