
28-04-08

18:57
Οι δύο πρώτες ήταν εκτός της ύλης που έκανα πέρυσι, για αυτό δε μπορώ να σε βοηθήσω.
63/73:
α)(1):αιθένιο (2):υδρογόνο
Από τα δεδομένα της άσκησης βγάζουμε: nολ=n1+n2 Το nολ το βρίσκουμε από το δεδομένο των λίτρων του μίγματος σε STP->5mol (112/22.4=5)
Αναλύεις τα n1 και n2 σε m1/Mr1 και m2/Mr2 αντίστοιχα. Οι σχετικές μοριακές μάζες είναι γνωστές. Άρα έχεις την πρώτη εξίσωση.
Τη 2η την παίρνεις από το δεδομένο των 62γρ του μίγματος. m1+m2=62. Λύνεις το σύστημα και βγάζεις m1=56gr m2=6gr.
β)Τα 15,5γρ είναι το 25% του μίγματος Α άρα και οι επιμέρους ενώσεις στο μίγμα θα είναι 25% του αρχικού Άρα θα έχεις 14γρ(1)->0.5mol και 1,5γρ(2)->0.75mol
Η αντίδραση που γίνεται παρουσία Ni είναι μονόδρομη οπότε παίρνουμε 0,5mol->11.2L (0.5*22.4) αιθανίου(3) και περισσέυουν 0,25mol->5,6L υδρογόνου(1). Οι πόσότητες των αερίων (1)+(3) αποτελούν το μίγμα Β.
Αυτή όντως χρειαζόταν λίγο σκέψη, αλλά η 65 είναι εύκολη, προσπάθησέ την μόνος σου. Το βιβλιαράκι με τις λύσεις δεν το έχεις;
63/73:
α)(1):αιθένιο (2):υδρογόνο
Από τα δεδομένα της άσκησης βγάζουμε: nολ=n1+n2 Το nολ το βρίσκουμε από το δεδομένο των λίτρων του μίγματος σε STP->5mol (112/22.4=5)
Αναλύεις τα n1 και n2 σε m1/Mr1 και m2/Mr2 αντίστοιχα. Οι σχετικές μοριακές μάζες είναι γνωστές. Άρα έχεις την πρώτη εξίσωση.
Τη 2η την παίρνεις από το δεδομένο των 62γρ του μίγματος. m1+m2=62. Λύνεις το σύστημα και βγάζεις m1=56gr m2=6gr.
β)Τα 15,5γρ είναι το 25% του μίγματος Α άρα και οι επιμέρους ενώσεις στο μίγμα θα είναι 25% του αρχικού Άρα θα έχεις 14γρ(1)->0.5mol και 1,5γρ(2)->0.75mol
Η αντίδραση που γίνεται παρουσία Ni είναι μονόδρομη οπότε παίρνουμε 0,5mol->11.2L (0.5*22.4) αιθανίου(3) και περισσέυουν 0,25mol->5,6L υδρογόνου(1). Οι πόσότητες των αερίων (1)+(3) αποτελούν το μίγμα Β.
Αυτή όντως χρειαζόταν λίγο σκέψη, αλλά η 65 είναι εύκολη, προσπάθησέ την μόνος σου. Το βιβλιαράκι με τις λύσεις δεν το έχεις;

Σημείωση: Το μήνυμα αυτό γράφτηκε 16 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

29-12-07

21:13
Εξίσωση κάυσης: 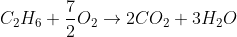
=2Ar(C)+6Ar(H)=2*12+6*1=30 (\frac{gr}{mol})\\n=\frac{m}{Mr}=\frac{3}{30}(mol)=0.1(mol))
To 1mol αιθανίου αντιστοιχεί σε 3mol νερού (όπως φαίνεται από την εξίσωση).
Τώρα έχουμε 0,1mol αιθανίου και ψάχνουμε τα xmol του νερού. Κάνουμε "χιαστί" και έχουμε x=0.3mol.
Τώρα:
1mol αντιστοιχεί σε 18mol, όμως τώρα έχουμε:
0,3mol που αντιστοιχούν σε y(gr) νερού. Κάνουμε "χιαστί" και έχουμε: 1*y=0.3*18 δηλ. y=5.4(gr)
Ελπίζω να ήμουν κατανοητός και προπαντός αναλυτικός!
To 1mol αιθανίου αντιστοιχεί σε 3mol νερού (όπως φαίνεται από την εξίσωση).
Τώρα έχουμε 0,1mol αιθανίου και ψάχνουμε τα xmol του νερού. Κάνουμε "χιαστί" και έχουμε x=0.3mol.
Τώρα:
1mol αντιστοιχεί σε 18mol, όμως τώρα έχουμε:
0,3mol που αντιστοιχούν σε y(gr) νερού. Κάνουμε "χιαστί" και έχουμε: 1*y=0.3*18 δηλ. y=5.4(gr)
Ελπίζω να ήμουν κατανοητός και προπαντός αναλυτικός!
Σημείωση: Το μήνυμα αυτό γράφτηκε 16 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

06-11-07

00:03
Ναι έχετε δίκιο, επειδή είμαι πάντα βιαστικός, δεν πρόσεξα καν τη λέξη "πειραματικά" και επειδή το βιβλίο έχει μία άσκηση μέσα με πειραματικά δεδομένα, αλλά δεν το αναφέρει (σελ. 73 ασκ. 58), νόμιζα ότι ξεχάσατε και εσείς να το διευκρινίσετε.
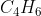 : Διπλασιάζω στα H τον αριθμό των ατόμων C και προσθέτω ή αφαιρώ έναν αριθμό έτσι ώστε να πετύχω τον πραγματικό αριθμό H.
: Διπλασιάζω στα H τον αριθμό των ατόμων C και προσθέτω ή αφαιρώ έναν αριθμό έτσι ώστε να πετύχω τον πραγματικό αριθμό H. 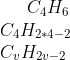 . Από ό,τι είχα δει πέρυσι κάποιοι συμμαθητές μου δεν το θεωρούσαν αυτονόητο.
. Από ό,τι είχα δει πέρυσι κάποιοι συμμαθητές μου δεν το θεωρούσαν αυτονόητο.
Επίσης θα ήταν πολύ καλό να προσθέσετε ένα παράδειγμα ολοκληρωμένο, για να το έχουν πάντα ως πρότυπο.
Κάτι που θα πρόσθετα εγώ σε αυτό είναι το πώς βρίσκουμε το ΓΜΤ της ομόλογης σειράς στην οποία ανήκει η ένωση: πχΘα με ενδιέφερε η άποψή σου και στους κανόνες. Βοηθάνε έτσι όπως είναι γραμμένοι?
Επίσης θα ήταν πολύ καλό να προσθέσετε ένα παράδειγμα ολοκληρωμένο, για να το έχουν πάντα ως πρότυπο.
Σημείωση: Το μήνυμα αυτό γράφτηκε 16 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

05-11-07

20:54
Στο τέλος εκεί που έχετε μερικές ασκήσεις για εξάσκηση, δίνετε: Η Mr μιας αλκοόλης είναι 90. Να βρεθεί ο ΜΤ και τα ισομερή του (κάπως έτσι τέλος πάντων).
Δεν μπορεί να είναι αυτή η Mr (εκτός και αν κάνω λάθος βέβαια), γιατί ο v δεν βγαίνει φυσικός αριθμός στον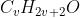 .
.
ΈχουμεArH+ArO=14v+18)
Όμως: Mr=90, οπότε:
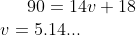
Δεν μπορεί να είναι αυτή η Mr (εκτός και αν κάνω λάθος βέβαια), γιατί ο v δεν βγαίνει φυσικός αριθμός στον
Έχουμε
Όμως: Mr=90, οπότε:
Σημείωση: Το μήνυμα αυτό γράφτηκε 16 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

30-10-07

12:02
Κύριε καθηγητά, ελέγξτε αν τα έχω κάνει σωστά:
1/μεθ-αν-ιο, 2/αιθ-εν-ιο, 3/πεντ-αν-ιο, 4/μεθ-αν-ολη, 5/αιθ-αν-ιο, 6/προπ-εν-ιο, 7/πεντ-εν-ιο, 8/αιθ-αν-ολη, 9/προπ-αν-ιο, 10/βουτ-εν-ιο, 11/πεντ-2-εν-ιο, 12/προπ-αν-ολη, 13/βουτ-αν-ιο, 14/βουτ-2-εν-ιο, 15/πεντ-2-εν-ιο, 16/εξ-3,5-διεν-ολη, 17/εξ-αν-ικο οξυ, 18/ πεντ-αν-2-ονη, 19/εξ-εν-4-ιν-3-ολη, 20/μεθ-αν-ικο οξυ, 21/προπ-αν-αλη, 22/επτ-4-εν-2-ονη, 23/βουτ-αν-αλη, 24/πεντ-2-εν-4-ιν-ιο, 25/μεθ-αν-αλη, 26/πεντα-1,4-διεν-3-ολη, 27/πεντ-3-ιν-ολη, 28/πεντ-εν-4-ιν-ιο, 29/3-μεθυλο-εξ-5-ιν-ιο, 30/μεθ-αν-ικο οξυ, 31/βενζολιο, 32/πεντ-3-ιν-2-ονη, 33/πεντ-αν-3-ονη, 34/2-μεθυλο-πεντ-αν-αλη.
Είναι πιθανόν να υπάρχουν λάθη όπως: αντί -ολη -> -αλη ή και το αντίστροφο που όμως δεν ευθύνονται στο ότι δεν τα ήξερα, αλλά στο ότι δεν ξεχώριζα τι έγραφα. Επίσης ίσως να υπάρχει και κανένα λάθος στους δεσμούς: (εν<->ιν). Τέλος, ίσως να υπάρχουν και λάθη στην "ακουστική" των λέξεων, όπως: αντί 1,4,3-πενταδιενολη -> 1,4,3-πεντδιενολη. Όλα αυτά όμως είναι λάθη απροσεξίας, δε μετράνε...
Τα έγραψα με το πιο αναλυτικό τρόπο που γίνεται, για να είναι κατανοητή η ονομασία και στους μαθητές της 2ας που ίσως να μην έχουν εξοικειωθεί ακόμα με την ονοματολογία (πχ το 26 θα μπορούσα να το γράψω: 1,4,3-πενταδιενολη)
1/μεθ-αν-ιο, 2/αιθ-εν-ιο, 3/πεντ-αν-ιο, 4/μεθ-αν-ολη, 5/αιθ-αν-ιο, 6/προπ-εν-ιο, 7/πεντ-εν-ιο, 8/αιθ-αν-ολη, 9/προπ-αν-ιο, 10/βουτ-εν-ιο, 11/πεντ-2-εν-ιο, 12/προπ-αν-ολη, 13/βουτ-αν-ιο, 14/βουτ-2-εν-ιο, 15/πεντ-2-εν-ιο, 16/εξ-3,5-διεν-ολη, 17/εξ-αν-ικο οξυ, 18/ πεντ-αν-2-ονη, 19/εξ-εν-4-ιν-3-ολη, 20/μεθ-αν-ικο οξυ, 21/προπ-αν-αλη, 22/επτ-4-εν-2-ονη, 23/βουτ-αν-αλη, 24/πεντ-2-εν-4-ιν-ιο, 25/μεθ-αν-αλη, 26/πεντα-1,4-διεν-3-ολη, 27/πεντ-3-ιν-ολη, 28/πεντ-εν-4-ιν-ιο, 29/3-μεθυλο-εξ-5-ιν-ιο, 30/μεθ-αν-ικο οξυ, 31/βενζολιο, 32/πεντ-3-ιν-2-ονη, 33/πεντ-αν-3-ονη, 34/2-μεθυλο-πεντ-αν-αλη.
Είναι πιθανόν να υπάρχουν λάθη όπως: αντί -ολη -> -αλη ή και το αντίστροφο που όμως δεν ευθύνονται στο ότι δεν τα ήξερα, αλλά στο ότι δεν ξεχώριζα τι έγραφα. Επίσης ίσως να υπάρχει και κανένα λάθος στους δεσμούς: (εν<->ιν). Τέλος, ίσως να υπάρχουν και λάθη στην "ακουστική" των λέξεων, όπως: αντί 1,4,3-πενταδιενολη -> 1,4,3-πεντδιενολη. Όλα αυτά όμως είναι λάθη απροσεξίας, δε μετράνε...

Τα έγραψα με το πιο αναλυτικό τρόπο που γίνεται, για να είναι κατανοητή η ονομασία και στους μαθητές της 2ας που ίσως να μην έχουν εξοικειωθεί ακόμα με την ονοματολογία (πχ το 26 θα μπορούσα να το γράψω: 1,4,3-πενταδιενολη)
Σημείωση: Το μήνυμα αυτό γράφτηκε 16 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

26-10-07

23:07
Όπως λέει και ένας καθηγητής μου, είμαστε χημικά ρομπότ.ακόμα και ο τρόπος που σκεφτόμαστε είναι χημεία! Οι πληροφορίες ο εγκέφαλος τις αποθηκεύει κάνοντας Χημεία και πολλά ακόμα.
Σημείωση: Το μήνυμα αυτό γράφτηκε 16 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.

25-10-07

22:44
Όχι, δεν είναι σωστό. Πρέπει να βάλεις και το πρώτο δυάρι, για να δηλώσεις το που βρίσκεται η διακλάδωση.αιθυλο-2προπενολη?
Σημείωση: Το μήνυμα αυτό γράφτηκε 16 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
-
Το forum μας χρησιμοποιεί cookies για να βελτιστοποιήσει την εμπειρία σας.
Συνεχίζοντας την περιήγησή σας, συναινείτε στη χρήση cookies στον περιηγητή σας.
 Αρχική Forum
Αρχική Forum
 Ρωτήστε κάτι
Ρωτήστε κάτι
 Προσωπικές Συζητήσεις
Προσωπικές Συζητήσεις
 Πανελλαδικές
Πανελλαδικές
 Αγγελίες
Αγγελίες
 Chat
Chat
 Συνδεδεμένοι Χρήστες
Συνδεδεμένοι Χρήστες
 Λίστα Αποκλεισμένων
Λίστα Αποκλεισμένων
 Υπεύθυνοι του Forum
Υπεύθυνοι του Forum
 e-steki
e-steki