

Εδώ μπορείτε να βρείτε τα ένθετα που κυκλοφόρησαν ( δωρεάν ) τρείς ( τέσσερις ) συγγραφείς σχολικών βοηθημάτων και που δίνονται δωρεάν μιας που η ενότητα των "παραγόντων της ταχύτητας αντίδρασης / Καταλύτες" μπήκε καλοκαιριάτικα στην εξεταστέα ύλη και δεν πρόλαβε να ενσωματωθεί στις υπάρχουσες εκδόσεις.
Καλό διάβασμα .
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Ν2 + Ο2 <=> 2 ΝΟ
ή
Ν2 + 2 Ο2 <=> 2 ΝΟ2
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Γι’ αυτόν τον λόγο υπάρχουν οι εμπειρικοί κανόνες …
Εάν όμως η ένωση είναι οργανική ( κλασική περίπτωση ομοιοπολικής ένωσης ) θα πρέπει να γράψεις τον αναλυτικό συντακτικό τύπο ( που εδώ τον γνωρίζεις ) και να βρεις τον ΑΟ για κάθε στοιχείο ξεχωριστά. Ειδικά στην περίπτωση του C τα πράγματα αποκτούν ιδιαίτερο ενδιαφέρον μιας που κάθε άτομο C μπορεί να έχει άλλο ΑΟ ( δες το παράδειγμα του σχολικού με το CH3CH2CH3 )
Θα σου είναι ιδιαίτερα χρήσιμο στις αντιδράσεις οξειδοαναγωγής της οργανικής χημείας.
ΥΓ όσο αναφορά τον «πράσινο» Σαλτερή ( ή τον «κόκκινο» της έκδοσης του 2017 ) δεν έχει ενότητα που έχει προστεθεί φέτος ( δες εδώ )
Επειδή μάλλον δεν θα βρεις κανένα βοήθημα που να την έχει σου προτείνω να κατεβάσεις τις σημειώσεις των Λατζώνη-Κονδύλη ( που προσφέρονται δωρεάν εδώ ) και να διαβάσεις από εκεί. Σε περίπτωση που δεν καλυφθείς ( δεν το νομίζω ) μπορώ να σου στείλω και τις δικές μου σημειώσεις .
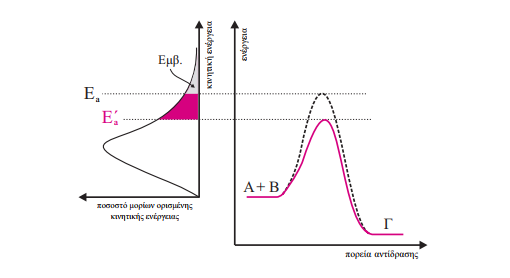
Οι παράγοντες της ταχύτητας της αντίδρασης/καταλύτες επηρεάζουν και την ταχύτητα των αμφίδρομων αντιδράσεων ( ενότητα ΧΙ ) .
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Η διατύπωση της έκφρασης της Kc είναι ανεξάρτητη από την φορά εκδήλωσης της αντίδρασης ( ή την φορά μετατόπισης της θέσης ισορροπίας ) και εξαρτάται ΑΠΟΚΛΕΙΣΤΙΚΑ από την χημική εξίσωση που ( ο εκφωνητής ) περιγράφει το φαινόμενο ( εδώ αντίδραση )
Η παρανόηση οφείλεται εν μέρει σε εμάς τους εκπαιδευτικούς που για λόγους ( μάλλον ) ταχύτητας ή συνήθειας αποκαλούμε τις ουσίες που βρίσκονται στα δεξιά ως «προϊόντα» και τις ουσίες που γράφονται αριστερά ως «αντιδρώντα» , την ίδια στιγμή που μιλάμε για δύο ταυτόχρονα (και αντίθετα) εξελισσόμενες αντιδράσεις που όλες οι ουσίες είναι αντιδρώντα και προϊόντα . ( βλέπεις το παράδοξο ?)
Για να συνδυάσεις τα παραπάνω θυμήσου την διαφορά της έκφρασης της Κc που περιγράφει δύο ισοδύναμες εκφράσεις χημικής εξίσωσης πχ την Α <=> 2 Β και την ½ Α <=> Β.
Η έκφραση της Kc είναι μία και αφορά την χημική εξίσωση που έχει ( την υποχρέωση να ) θέσει ο εκφωνητής. Θα έπρεπε να σου κάνει εντύπωση ότι σε όλες τις ασκήσεις ΧΙ η χημική εξίσωση που περιγράφει την αμφίδρομη αντίδραση είναι διατυπωμένη από τον εκφωνητή.
Πρόσεξε ‘το για είναι κλασικό λάθος ( και συνηθισμένο σημείο ελέγχου γνώσεων )
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Θα έπρεπε να γράφει ότι όταν η πίεση στο δοχείο σταθεροποιείται , στο δοχείο περιέχονται 1,5 mol ουσίας Γ
Σημείωση: Το μήνυμα αυτό γράφτηκε 6 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Σημείωση: Το μήνυμα αυτό γράφτηκε 7 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Υγ .... συμφωνώ και εγώ . Η θεωρία Bohr , ο υβριδισμός και η παράγραφος της Θερμοχημείας θα μπορούσαν να είναι στην Β Λυκείου ( στο μάθημα Γενικής Παιδείας ή σε μάθημα κατεύθυνσης )
υγ ... ξεχασα να αναφέρω την πηγή της στατιστικής μελέτης του προήγούμενου ποστ . Είναι από εδώ
υγ ... από το ίδιο blog ... ορίστε μια γενικότερη μελέτη της απόδοσης στην Χημεία
Σημείωση: Το μήνυμα αυτό γράφτηκε 7 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Γενική θεματοδοσία ανα παράγραφο :

Ειδικότερα στην θεωρία :

Και στις ασκήσεις :

Συνολικά :

Καλή συνέχεια στο διάβασμα .
Σημείωση: Το μήνυμα αυτό γράφτηκε 7 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Σημείωση: Το μήνυμα αυτό γράφτηκε 8 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.



Για το 2ο ( εκει με την αλογονοφορμική ... τι να σου πώ .... πως το κατάφερες αυτό
 ..... δεν γνωρίζω ... μάλλον θα το συζητήσουν μέσα στην αίθουσα διόρθωσης ... πάντως κάτι θα κερδίσεις
..... δεν γνωρίζω ... μάλλον θα το συζητήσουν μέσα στην αίθουσα διόρθωσης ... πάντως κάτι θα κερδίσεις
Σημείωση: Το μήνυμα αυτό γράφτηκε 9 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


( μην μου το κάνεις αυτό .... δεν θέλω να διαπιστώνω ιντερνετικά κομμένα μόρια εξετάσεων )
Σημείωση: Το μήνυμα αυτό γράφτηκε 9 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Εκτιμώ ότι ο συνδυασμός της χρησιμοποιήσης της υδρόλυσης ( και όχι της σαπωνοποίησης ) του εστέρα + την μη αναγραφή της οξείδωσης του CH3OH που δίνει και αυτή το προιον που επικαλείσαι θα σου κόψει 1 μονάδα
Αυτή είναι η προσωπική που εκτίμηση .... η διόρθωση αρχίζει αύριο ( δεν θα είμαι φέτος διορθωτής ) και την 1η ημέρα συζητιούνται τέτοιες περιπτώσεις. ( ενώ η κανονική ροή της διόρθωσης θα αρχίσει την Τετάρτη ). Αν μάθω κάτι από μέσα θα σου πω με pm
Σημείωση: Το μήνυμα αυτό γράφτηκε 9 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Σημείωση: Το μήνυμα αυτό γράφτηκε 9 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Σημείωση: Το μήνυμα αυτό γράφτηκε 10 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


ΗΑ (+) Β <=> Α- (+) ΒΗ+
Η μεταφορά του πρωτονίου γίνεται από το οξύ ( δότης , ) πρός την βάση ( δεκτης )
Οι ιοντισμοί ( πλήρεις και μερικοί ) είναι πρωτολυτικές αντιδράσεις .

Σημείωση: Το μήνυμα αυτό γράφτηκε 10 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Το προσωπικό μου blog με θέματα Χημείας ( προσανατολισμένο κυρίως στις Πανελλήνιες Εξετάσεις )
Προσθέτω ανάρτηση περίπου ανά 15 ημέρες και θέλω να πιστεύω ότι θα σας βοηθήσει .
Σημείωση: Το μήνυμα αυτό γράφτηκε 10 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


ΚαλησπεραΚανω θερινα μαθηματα σε φροντιστηριο (Θετικη Κατευθυνση) και γραψαμε διαγνωνισμα στη Χημεια Κατευθυνσης και ελυσα ο,τι ειχε και δεν ειχε περα απο μια ασκηση που καθομουνα και εσπαγα το κεφαλι μου. Τα διαγωνισματα θα τα παρουμε οταν ξαναρχισουμε. Μεχρι τοτε εχουμε να κανουμε φυλλαδια για καθε μαθημα. Τυχαινει, λοιπον, η πρωτη ασκηση να ειναι αυτη που δεν μπορεσα να λυσω...
Θα το εκτιμουσα πολυ αν μπορουσε καποιος να με βοηθησει μιας και οι διακοπες τελειωνουν και τα περιθωρια για την παραδοση της εργασιας στενευουν... Η εκφωνηση: Οταν ενα ηλεκτρονιο του ατομου του υδρογονου μεταπιπτει απο τη στιβαδα N στη στιβαδα L εκπεμπεται φωτονιο με μηκος κυματος λ1. Οταν ενα ηλεκτρονιο του ατομου του υδρογονου μεταπιπτει απο τη στιβαδα L στη στιβαδα K εκπεμπεται φωτονιο με μηκος κυματος λ2. Να υπολογισετε το λογο λ1/λ2.
Ευχαριστω προκαταβολικα οποιονδηποτε μπορει να βοηθησει
… κατ’αρχάς , να σου πω πως πρέπει να προβληματιστείς για την άσκηση που δεν μπόρεσες να λύσεις, μιας που είναι κλασικότατη και δείχνει ότι μάλλον κάτι δεν έχεις καταλάβει καλά στο θέμα του ατομικού προτύπου Bohr
Για να βοηθήσω επιγραμματικά σου λέω ότι η ενέργεια του εκπεμπόμενου φωτονίου είναι ίση με την διαφορά ενέργειας ανάμεσα στις στιβάδες που γίνεται η μετάπτωση ( αποδιέγερση )
Κατά την αποδιέγερση λοιπόν :
ΕΦ = ΔΕΑΠΟΔΙΕΓΕΡΣΗΣ = ΕΑΡΧ – ΕΤΕΛ ( αρχή διατήρησης της ενέργειας )
Επίσης ΕΦ = h*f = h*c/λ
…. Στην απορία σου …

Εάν θες λύσε την παρακάτω παραλλαγή της παραπάνω άσκησης για να ελέγξεις εάν κατανόησες το φαινόμενο …
Το ηλεκτρόνιο του ατόμου του υδρογόνου έχει διεγερθεί στην στιβάδα Ο. Κατά την αποδιέγερση του μεταπίπτει πρώτα στην στιβάδα Χ εκπέμποντας φωτόνιο 1 και μετά ( από την στιβάδα Χ ) στην θεμελιώδη κατάσταση εκπέμποντας φωτόνιο 2 αντίστοιχα. Εάν οι συχνότητες των δύο φωτονίων έχουν λόγο f_1/f_2 =7/25 , να βρεθεί ποια είναι η στιβάδα Χ.
Σημείωση: Το μήνυμα αυτό γράφτηκε 10 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Σημείωση: Το μήνυμα αυτό γράφτηκε 10 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


υγ .... Ο Κουλιφέτης είναι τριςμέγιστος δάσκαλος Χημείας αλλά στο θέμα του "Mr Black" είναι - ΙΜΟ - υπερβολικός . ( βεβαια το περσινό 4ο θέμα ήταν εντελώς βλακώδες )
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Η φρίκη που σε έχει πιάσει για την σειρά δραστικότητας των καρβονυλικών ενώσεων ( στα προσθήκη των Grignard ) .... στην υποκατ΄σταση των RX .... είναι προς την σωστή κατεύθυνση

υγ ... διαβασε για το pH=7 της σελ 252
+ στην προσομοίωση επεσε το 2ο σταδιο της αλογονοφορμικής ως ανεξάρτητη αντίδραση ( take a look )
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


μπορει να τεθει καποιο ερωτημα (στα πολλαλπης επιλογης) σχετικα με σταθεροτητα αλκενιων????
.... όλα τα αλκένια ( της Γ Λυκέιου ) είναι σταθερά. ( μην το συνδέεις με τον κανόνα Μαρκοβνικοβ που φανερώνει πιθανότερες μορφές σε συγκεκριμένη μέθοδο παρασκευής )
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Κάτσε δεν κατάλαβα, αφού μας δείνει όγκους. Με αυτούς τους όγκους το μέγιστο που μπορεί να δημιουργηθεί;
Δεν μας δίνει τους όγκους που θα χρησιμοποιηθούν .... μας δίνει τους ( μέγιστους ) όγκους που μπορούν να χρησιμοποιηθούν .
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Οι ασκήσεις μέγιστου όγκου λύνονται με την μεθοδολογία ασκήσεων αναλογίας όγκου.
Εστω V1 από το Δ1 και V2 από το Δ2 .... κατά τα γνωστά καταλήγουμε V1/V2=1/4
Για να προκύψει ο μέγιστος όγκος στο τελικό διάλυμα ( που είναι ρυθμιστικό ) θα πρέπει να χρησιμοποιηθεί πλήρως τουλάχιστον ένα από τα δύο διαλύματα.
Εάν χρησιμοποιηθεί πλήρως το Δ1 δηλ V1=400 απαιτούνται 4*400=1600 από το V2 ( που δεν έχουμε άρα άτοπο )
Εάν χρησιμοποιηθεί πλήρως το Δ2 δηλ V2=400 απαιτούνται 400/4=100 από το V2 ( που έχουμε )
Αρα συνολικά το σενάριο μπορεί να δώσει μέγιστο όγκο τελικού διαλύματος, έχει 400+100=500 mL
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Όταν ο C συμμετέχει σε 1 τριπλό δεσμό ---> φτιάχνει τους σ δεσμούς του με 2 υβριδισμένα τροχικά τύπου sp που σχηματίζουν μεταξύ τους γωνία 180 μοίρες ---> έτσι ο C και τα δύο άλλα άτομα που είναι ενωμένα με αυτόν μέσω αυτών των δεσμών είναι στην ίδια ευθεία
Όταν ο C συμμετέχει σε 1 διπλό δεσμό ---> φτιάχνει τους σ δεσμούς του με 3 υβριδισμένα τροχικά τύπου sp2 που σχηματίζουν μεταξύ τους γωνία 120 μοίρες και είναι και στο ίδιο επίπεδο ( σαν το σήμα της Μερσεντες ) ---> έτσι ο C και τα τρία άλλα άτομα που είναι ενωμένα με αυτόν μέσω αυτών των δεσμών είναι στο ίδιο επίπεδο και σε γωνία 120 μοίρες
Όταν ο C συμμετέχει σε μόνο απλούς δεσμούς ---> φτιάχνει τους σ δεσμούς του με 4 υβριδισμένα τροχικά τύπου sp3 που σχηματίζουν μεταξύ τους γωνία 108 μοίρες και είναι στις γωνίες μιας τριγωνικής πυραμίδας , ---> έτσι οι δεσμοί είναι πάνω στις ευθείες που ενώνουν το κέντρο της πυραμίδας ( που είναι ο C ) με τις 4 κορυφές της πυραμίδας ...
Tips
Κάθε φορά που μελετάς μια ένωση ,
- ξεκίνα από τα άτομα C του διπλού δεσμού ( τα 2 άτομα C και τα 4 άλλα άτομα που είναι ενωμένα με αυτά είναι στο ίδιο επίπεδο ) ...
- Τα δύο άτομα C του τριπλού δεσμού και τα 2 άλλα άτομα που έίναι ενωμένα με αυτά είναι στην ίδια ευθεία ....
- Τρία σημεία ορίζουν ένα επίπεδο ( γεωμετρικός κανόνας )
- στο COOH , -CO- , -CHO υπάρχει "κρυμμένος" διπλός δεσμός C=O
- στο CN .... υπάρχει τριπλός δεσμός
υγ .... πήγαινε στην σελίδα https://jmol.sourceforge.net/ και κατέβασε το java applet ... ( από εδώ https://jmol.sourceforge.net/download/ ) .... τρέξε το jmol ( είναι executable java file ) .... μην χάσεις πάνω από μια ώρα σε αυτό .... αν τα καταφέρεις ... καλώς ....
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Παράδειγμα .... η p υποστιβάδα είναι το σύνολο 3 τροχιακών που έχουν κοινό σχήμα ( αυτό του αλτήρα / βαράκι ).
Η s υποστιβάδα είναι το συνολο 1 τροχιακού που είναι σφαιρικό. Και επειδή το "συνολο 1 τροχιακού" είναι ουσιαστικά 1 τροχιακό => η έννοια της s υποστιβάδας και του τροχιακού της ..... ταυτίζονται . ( φαντάσου μια ομάδα σε ένα ατομικό άθλημα .... πόσα μέλη έχει .... 1 ..... 1 αθλητής .... 1 ομάδα )
Η στιβάδα L έχει 2 είδη τροχιακών ( δηλ δύο είδη εικόνων που θα προκύψουν εαν πραγματικά υπάρξουν e σε αυτήν ) .... τα σφαιρικά και τα βαράκια .... το 1 σφαιρικό συγκροτεί την υποστιβάδα s και τα 3 βαράκια συγκροτούν την υποστιβάδα p .... εάν δούμε καλύτερα τα νεφη της υποστιβάδας p θα δούμε ότι είναι 3 .... ίδια .... αλλά με διαφορετικό προσανατολισμό ( χ , ψ , ζ ) ....
Η στιβάδα Μ έχει 3 είδη τροχιακών .... σφαίρες .... βαράκια .... πιπίλες ( μην γελάς ) ....που προφανώς διαφέρουν στο σχήμα τους . Αρα έχει 3 είδη υποστιβάδων .... που διαφέρουν τα p τροχιακά της L από αυτά της M ?.... έχουν ίδιο σχήμα ? ναι ... προσανατολισμούς ?...ναι ..... διαφέρουν στην τάξη μεγεθους. ( άρα και στην ενέργεια )
Όλα αυτά μπορείς να τα προβλέψεις χρησιμοποιώντας τους κανόνες/περιορισμούς που έχουν οι κβαντικοί αριθμοί .... για n=2 ( στιβάδα L ) ....το l παίρνει δύο τιμές ( 0 , 1 ) ... δηλάδή δύο υποστιβάδες ( δύο είδη τροχιακών ) ... το πρώτο είδος ( το s ) έχει 1 τροχιακό .... το άλλο είδος ( το p ) έχει 3 τροχιακά ( γιατί με l=1 ... το ml που φανερώνει προσανατολισμούς σε είδη τροχιακών παίρνει 3 τιμές ).... κτλ κτλ
Τα τροχικά που ανήκουν στο ίδιο είδος , σε κάθε στιβάδα .... δηλ τα τροχιακά της κάθε υποστιβάδας μιας στιβάδας ... έχουν την ίδια ενέργεια ... αρα και τα ηλεκτρόνια που θα τρέξουν στον χώρο τους θα έχουν την ίδια ενέργεια ... εάν όμως μιλάμε για το άτομο του Η να ξέρεις ότι τα διαθέσιμα τροχικα της ίδια στιβάδας έχουν ίδια ενέργεια ... δηλ σε πολυατομικό άτομο η ενέργεια 2s<2p ( αρα στα τροχιακά 2s<2px=2py=2pz ) ένώ στο Η ... 2s=2p ( άρα στα τροχιακά 2s=2px=2py=2pz )
Τωρα πρόσεξε την παγίδα .... παρόλο που τα ( το ) τροχιακό της 4s < 3d ( άρα θα συμπληρωθεί πρώτα το 4s ) ... εάν συγκρίνουμε την ενέργεια των ηλεκτρονιών 4s vs 3d .... τότε 3d<4s .... γιατί με το που θα μπουν ηλεκτρόνια στην 4s αυτά θα αποκτήσουν μεγαλύτερη ενεργεια από τα επόμενα που θα μπούν στην 3d ( αλλά θα έχουν ηδη προλάβει να μπεί )
Τελικά ... να εξηγείς θεωρίες μέσα από πληκτρολόγιο είναι πολύ δύσκολο .... ελπίζω να βοηθησα ...
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


https://users.sch.gr/kassetas/educ287.htm
Πρόσεξε ότι αντιμετωπίζει το "τροχιακό" ως μια συνάρτηση ( δηλ χωρίς φυσικό νόημα ) που ΘΑ σε βοηθήσει να αποκτήσεις εικόνα για το που βρίσκετε ένα ηλεκτρόνιο .... και επειδή δεν θα μπορέσεις ΠΟΤΕ να απαντήσεις απολύτως στο συγκεκριμένο ερώτημα ( βάση της απροσδιοριστίας που είναι έν γέννη ιδιότητα της φύσης ) ... θα σε σε βοηθήσει να ΠΙΘΑΝΟΛΟΓΉΣΕΙΣ ( μέσω του ψ^2 ) ... να ξέρεις επίσης ότι θα μπορέσεις να ΟΠΤΙΚΟΠΟΙΗΣΕΙΣ την πιθανότητα αυτή μόνο εάν υπάρξουν ηλεκτρόνια στις περιοχές αυτές που η συναρτηση του ατομικού τροχιακού πιθανολογεί.
Αξίζει να διαβάσετε όλη την προσέγγιση του Ανδρ. Κασσέτα για την κβαντική προσέγγιση της ατομικής θεωρίας της Χημείας Κατεύθυνσης ..... εδώ --> https://users.sch.gr/kassetas/educ28.htm
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


δν μου δινει ομως την ka του hb...αν και νομιζω πως βγαινει και χωρις αυτην
ok .... πρωτα πρώτα να σου πώ ότι η συγκεκριμένη άσκηση ήταν το 4ο θέμα τοων δεσμών το 1998 ( και θεωρείται από τα καλύτερα θέματα ιοντικής που έχουν πέσει ..... και βεβαια ΞΑΝΑγραφω ότι εξουδετέρωση μιγματων - μερική ή ολική θεωρείται ΣΟΣ για φέτος )
Στην συγκεκριμένη άσκηση από την Κ του ΗΑ θα βρείς τα [H3O+] και μετά θα πας να βρείς την Κ του ΗΒ για να κάνεις συγκριση ισχύος ...
ΥΓ .... ανεβάζω σε επισύναψη την λύση που δίνει ένα φροντιστηριο ( και την αποδέχομαι πλήρως ) για το θέμα του 1998
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Συνημμένα


Υπάρχουν 3 κοινά ιόντα [Α-]=C1+x=C1 .... [B-]=C2+y=C2 ..... [H3O+]=x+y ( εδώ όχι προσέγγιση )
Γραψε τις δύο Κ και ( εγώ σου προτείνω ) να διαιρέσεις κατά μέλη και να βρείς μια σχέση ανάμεσα στο χ και στο y .... μετά πήγαινε στο [Η3Ο+] και γράψε το σε σχέση με το χ ( ή το y ) μόνο .... και μετά σε μια Κ .... βρίσκεις το χ .... βρίσκεις το y .... βρίσκεις το Χ+Y δη΄λ την [H3O+] .... και το pH...
Σε διάφορα βοηθήματα θα βρείς να προσθέτουν της δύο Κ και να βρίσκουν - πρώτα - το [Η3Ο] ( στο τετράγωνο ) και μετά το pH ....
Και οι δύο τρόποι είναι σωστοί , ... αυτός που σου πρότεινα βρίσκει και το χ και το y .... άρα και τους βαθμούς ιοντισμού των ΗΑ και ΗΒ ....
Δοκίμασε το στην άσκηση που δίνεις ( σε αυτήν μην ξεχάσεις να χωρίσεις - αρχικά - 80%*0,5=0,4 mol NaOH για την αντίδραση με το ΗΑ και 20%*0,5=0,1 mol για την αντίδραση με το ΗΒ ...
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


εθοδολογια π ακολουθουμε για επιλυση ασκησης με τριπλη επιδραση κοινου ιοντος??
.... επειδη αυτοό το "τριπλή επίδραση ιόντος" δεν το αντιλαμβάνομαι ..... μπορείς να δώσεις ένα παράδειγμα διαλύματος ?
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Επειδή βλέπω πως ο βασσιλάκος δεν είναι ονλάιν, θα σε βοηθήσω!
είναι χ CO2 . ψ/2 νερά.
στα αντιδρώντα βάζεις (2χ+ψ/2)/2 O2
Στην ουσία το μόνο που κάνεις είναι να προσέχεις να έχεις τα ίδια άτομα και στα 2 μέλη.
Fixxed
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


... από την μάζα του μίγματος προκύπτουν 0,3 mol NaHSO4 και 0.3 mol Na2SO4 άρα η συγκέντρωση θα γίνει 0,6 Μ για κάθε ουσία.
Διαστάσεις
NaHSO4 --> Na + HSO4
Mένουν - 0,6 0,6
Na2SO4--> 2 Na + SO4
Mένουν - 1.2 0.6
Ιοντισμοί ιόντων που προέρχονται από άλατα ( έλεγχος για υδρόλυση )
HSO4 + Η2Ο <=> SO4 + H3O
Μένουν 0,6-x x x
ΕΚΙ : [SO4]=0,6+x = 0,6 ( για να μην τεθεί θέμα προσεγγίσεων λόγω της μεγάλης Κ = 0,01 ... o Σαλτερής ονομάζει το διάλυμα "ρυθμιστικό" για να κάνεις προσεγγίσεις )
Κa(HSO4)=Ka2 = x*0.6 / 0.6 => x = 0.01 => pH=2
ΠΡΟΣΟΧΗ .... στο συνημμένο αρχείο θα βρείς γιατί το HSO4 παρόλο που μοιάζει με ιόν που έχει αμφιπρωτική συμπεριφορά ... δρά μόνο ως οξύ.
17*101
Οι ασκήσεις μέγιστου όγκου λύνονται με την μεθοδολογία ασκήσεων αναλογίας όγκου.
Εστω V1 από το Δ1 και V2 από το Δ2 .... κατά τα γνωστά καταλήγουμε V1/V2=1/4
Για να προκύψει ο μέγιστος όγκος στο τελικό διάλυμα ( που είναι ρυθμιστικό ) θα πρέπει να χρησιμοποιηθεί πλήρως τουλάχιστον ένα από τα δύο διαλύματα.
Εάν χρησιμοποιηθεί πλήρως το Δ1 δηλ V1=400 απαιτούνται 4*400=1600 από το V2 ( που δεν έχουμε άρα άτοπο )
Εάν χρησιμοποιηθεί πλήρως το Δ2 δηλ V2=400 απαιτούνται 400/4=100 από το V2 ( που έχουμε )
Αρα συνολικά το σενάριο μπορεί να δώσει μέγιστο όγκο τελικού διαλύματος, έχει 400+100=500 mL

Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
Συνημμένα


sp3 => πυραμίδα - 109
sp2 => τρίγωνο / επίπεδο - 120
sp => ευθεία - 180
Είναι πολύ λίγα για να σε απασχολήσουν .... ειδικά εφόσν δίνεις για 2η φορά .... δεν αξίζει να μην τα μάθεις και να μην κοιμάσαι ήσυχος το βράδυ των πανελληνίων ( είναι ανεπίτρεπτο να χάνεις μόρια θεωρίας ... ειδικά στην Χημεία των 50 σελίδων ... ειδικά εάν δίνεις 2η φορά )
Τα θέματα θεωρίας έχουν στερέψει επικινδυνα .... μην θεωρήσετε τίποτα -ΠΛΕΟΝ- τραβηγμένο να πέσει
Διαβάζουμε ΚΑΙ θεωρία Bohr .... ΚΑΙ ορισμούς κβαντικής θεωρίας .... ΚΑΙ παραδείγματα υβριδισμού ....
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


α) βρίσκεις τις c1 και c2 από τα επιμέρους ρυθμιστικά διαλύματα που έχουν τα πάντα γνωστά εκτός από τις ζητούμενες συγκεντρώσεις
β) βρίσκουμε τις νέες συγκεντρώσεις για τα ΗΑ και ΝαΑ μέσα από τον τύπο της ανάμειξης ( για V1=V2=V => Vτελ=2V)
πχ για την νέα συγκέντρωση του ΗΑ έχουμε 0,2*V1 + 0.2*V2 = C*Vτελ => 0,2*V + 0.2*V = Cτελ*2V => Cτελ=0,2
... ομοίως για το ΝαΑ .... κτλ ... ρυθμιστικό ΗΑ-ΝαΑ με τις νέες συγκεντρώσεις
.... 17*68
β) έστω V1 από το Δ1 και V2 από το Δ2
Ανάμειξη διαλυμάτων που τα συστατικά τους δεν αντιδρούν μεταξύ τους => μεθοδολογία νέων συγκεντρώσεων
ν'εα συγκέντρωση ΗΑ : (0,1*V1 + 0.3*V2) / V1 + V2 ..... ομοίως για το ΝαΑ .... από την σ΄χεση των νέων συγκεντρώσεων του ΗΑ με το ΝαΑ θα προκύψει η απάντηση για την σχέση V1/V2
YG ..... δεν απαντώ αμέσως για να σ΄φησω λίγο χρόνο στους "συμμαθητές σου" να σε βοηθήσουν με τον τρόπο τους
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


17*94γ .... αντίδραση NH4Cl + NaOH (μην ξεχάσεις ότι προυπάρχει ποσότητα ΝΗ3 ) ... έλεγχος "έστω πλήρη αντίδραση" ... ( το νέο pH είναι πάλι αυξημένο κατα 1 αφου΄προσθέτεις βάση που καταναλώνει οξύ ) ....
Πολύ καλή άσκηση ( ειδικά το γ )
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


1. χωρίζουμε τα ως προς εξέταση διαλύματα σε 3 κατηγορίες .... όξινα (Ο) ... ουδέτερα (ΟΥ) .... βασικά (Β). Το pH θα είναι Ο<ΟΥ<Β
2. Παίρνουμε μία μία τις κατηγορίες και κάνουμε συγκριση μεταξύ των διαλυμάτων που έχουμε συμπεριλάβει σε αυτές .
Πώς γίνεται αυτό ?
2Α ... ψάχνουμε για διαλύματα με ( ή που περιέχουν ) ισχυρούς ηλεκτρολύτες ( HCL - HNO3 - H2SO4 - NaOH - Ca(OH)2 ... )
Οι συγκεντρώσεις των ουσιών αυτών φανερώνουν άμμεσα και την συγκέντρωση των [Η3Ο+] ή [ΟΗ]
Προσοχή : #1 οι πολυπρωτικοί ηλεκτρολύτες ( μορφής Ca(OH)2 ) δίνουν πολλαπλάσια ΟΗ
Προσοχή : #2 το Η2SO4 είναι ισχυρό στο 1ο στάδιο ιοντισμού και ασθενές στο 2ο , έτσι ένα διάλυμα Η2SO4 0,1 Μ θα έχει [Η3Ο+] που θα είναι 0,1<[Η3Ο+]<0,2
2Β ... Στα διαλύματα που περιέχουν 1 ασθενή ηλεκτρολύτη η συγκριση γίνεται
α) μέσω C για διαλύματα της ίδιας διαλυμένης
β) μέσω Κ για διαλύματα διαφορετικών ουσιών που πρέπει όμως να έχουν την ίδια C
γ) εννοείται ότι ένα διάλυμα ισχυρού ΗΑ C M είναι πιο όξινο από κάθε διάλυμα ασθενούς ΗΒ ίδιας συγκέντρωσης
Επίσης ΕΝΝΟΕΙΤΑΙ ότι δεν πρέπει να υπάρχει ΚΑΝΕΝΑ θέμα με την αντιμετώπιση των διαλυμάτων αλάτων που κρύβουν όξινες ή βασικές ιδιότητες ( μέσω υδρόλυσης )
2Γ ... στα διαλύματα με τις 2 συζυγείς μορφές ( ρυθμιστικά )
α) για ίδια C1 της μορφής ΗΑ , όσο μεγαλύτερη είναι η C2 του ΝαΑ ( βάση) τόσο λιγότερο όξινο
β) τα διαλύματα με ίδιο πηλίκο C2/C1 των ίδιων μορφών έχουν ίδιο ph ( θα το δείς στα ρυθμιστικά ... δεν υπάρχει τέτοια περίπτωση στην 14*29 )
γ) εννοείται ότι ένα διάλυμα ΗΑ C M ... είναι πιο όξινο από ένα διάλυμα ΗΑ C M - NaA C' M , μιας που το 2ο έχει ίδια ποσότητα οξέος αλλά περιέχει και βάση ...
3. Βρες διαλύματα που μπορούν να ενώσουν μεγάλες ανισσότητες πχ αν α<β<ζ και ζ<ε<γ<δ τότε α<β<ζ<ε<γ<δ
Ελπίζω να βοήθησα ( σε γενικές γραμμές )
Για εξάσκηση στα παραπάνω σου προτείνω να λύσεις ΚΑΙ τις παρακάτω 2 ασκήσεις ( δεν πρόκειται να πέσουν όπως είναι αλλά κομμάτια τους είναι ΣΟΣ )


Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


για την 1. τους συντελεστες τους βαζω μαλλον κανω κατι λαθος στην ανντιδραση..Συγκεκριμενα :
nHCL = 9*10^-1 nCa(OH)2 = 2*10^-3 απο το προηγουμενο ερωτημα. Οποτε
Ca(OH)2 + 2HCL-> cACL2 + ΝΕΡΟ
αρχ.2*10^-3 9*10-3 -
Α/π 2*10^-3 το ιδιο το ιδιο
τελ. - 7 *10 ^-3 2*10^-3
.... δεν είναι το "το ιδιο"
η στοιχειομετρία "λέει" ότι το 1 mol Ca(OH)2 αντιδρα με 2 mol HCL
ΑΡΑ αφού (σωστά βρήκες ότι λόγω περίσσειας ) αντιδρούν τα 2*10^-3 mol Ca(OH)2 και ζητούν 2*2*10^-3 mol HCL
.... έτσι στο τελικό διάλυμα μένουν (9-2*2)*10^-3 mol HCL = 5 *10^-3 mol HCL και βέβαια λόγω του 1:1 παράγονται 2*10^-3 mol CaCL2
.... νέες συγκεντρώσεις ... ιοντισμός HCL .... διάσταση CaCL2 ... τσέκ για υδρόλυση στο αλάτι ... τσέκ για EKI ... τέλος.
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Οι συντελεστές είναι "όροι αναλογίας" και όχι "πολλαπλασιαστές ισότητας "
Τα 2 μολ HCl αντιδρούν με 1 mol Βα(ΟΗ)2
Τα 0,2 V............................ Χ
Χ=0,2V/2
όμως τα mol Βα(ΟΗ)2 είναι 0,05 V' άρα Χ=0,2V/2 = 0,05 V' => ... 1/2
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


Η αντίδραση έχει συντελεστή ....
2 ΗCL + Ba(OH)2 --> BaCl2 +2 H20
0.2 V από το HCL αντιδρά/ εξουδετερώνει πλήρως 0,2 V/2 άρα 0,2 V/2 = 0.05 V' => V/V'=1/2
.... προσέξτε τις αντιδράσεις με συντελεστές ( σοσ 2012-13). Έπεσαν πέρυσι στις επαναληπτικές ( RCOOH + Ca(oh)2 --> ) , υπάρχει άσκηση στο σχολικο βιβλίο ( Μg + CH3COOH --> ) και μπορεί να δώσει και ωραία ογκομέτρηση που δεν υπάρχει σε πολλά βοηθήματα ...
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


1. από την μία έχουμε λόγω της Αρχής Le Chatelier ( + mol CH3COONa ) μετατόπιση της Ι.Ι προς τα αριστερά
2. από την άλλη λόγω της προσθήκης νερού ( το CH3COONa προστίθεται με την μορφή διαλύματος ) - πάλι λόγω LeChatelier - μετατόπιση προς τα δεξιά
Ετσι δεν μπορούμε να γνωρίζουμε ποιος παράγοντας θα υπερισχύσει και ΔΕΝ μπορούμε να απαντήσουμε . Το ερώτημα ΔΕΝ μπορεί να υπάρξει αν και μπορώ να σου πω ότι για ανάμειξη στις γνώριμες τάξεις μεγέθους ( και παραπλήσιες συγκεντρώσεις ) ευνοείται ο 1ος παράγοντας ενώ όσο μεγαλύτερη είναι η αναλογία ανάμιξης και όσο πιο μικρή είναι η συγκέντρωση του CH3COONa ευνοείται ο 2ος παράγοντας.
Για να μην το κουράσω , το ερώτημα δεν μπορεί να υπάρξει για λυκειακό επίπεδο μιας που η λύση του απαιτεί την χρήση υποθετικού πηλίκου ( ανάλογου με το Qc της Χ.Ι ) που δεν γνωρίζουν οι μαθητές.
Για το pH εκτιμώ ότι η απάντηση είναι προφανής ...
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.


αναμειγνύουμε ισους ογκους κια συγκεντρώσεις των Na2CO3 και προκύπτει ρυθμιστικό διάλυμα?
Ναι έιναι ρυθμιστικό διάλυμα εφόσον έχεις μέσα στο διάλυμα τις μορφές HCO3- και CO3 = προερχόμενες από διαφορετικούς ηλεκτρολύτες . Φαντάζομαι ότι η ερώτηση σου πηγάζει από την αμφολυτική συμπεριφορά του HCO3- αλλά σου λέω ότι και σε αυτές τις περιπτώσεις ισχύει ο ορισμός των ρυθμιστικών διαλυμάτων. ( συγκεκριμένα το διάλυμα NaHCO3 - ΝαCO3 έχει πολύ εντυπωσιακή σταθερότητα στην αραίωση )
Με την ίδια σκέψη ΚΑΙ το διάλυμα ΝαΗSO4 - Na2SO4 είναι ρυθμιστικό διάλυμα. Εδώ βέβαια το HSO4-δεν μπορεί να δράσει ως βάση λόγω του ότι το H2SO4 είναι ισχυρό στον 1ο ιοντισμό του (ΘΕΜΑ 2012) έτσι τα πράγματα είναι πιο εύκολα ( και πιο ΣΟΣ )
Να σου πω όμως πληροφοριακά ότι επειδή το HSO4- έχει μεγάλη Κ ( ισχυρό οξύ ) το ρυθμιστικό που δημιουργεί με το NaHSO4 δεν αντέχει τόσο πολύ στις αραιώσεις
Καλημέρα , έχω απορία σε 3 ερωτήματα σε 3 διαφορετικές ασκήσεις..ελπίζω να μην κουράσω
1. 0,8 g Ca διαλύονται στο νερό, οπότε προκύπτει δ/μα Δ1 όγκου 4L. α) ποιό ειναι το PH του δ/τος Δ1; β) Σε 400 ml του Δ1 διαλύονται 100 ml υδατικού δ/τος HCL 0,09 M.Να υπολογίσετε το PH του Δ2 που προκύπτει ;
στο πρωτο ερωτημα εχω βρει κανονικα το PH = 12.. Το δευτερο ερωτημα με προβληματιζει δεν ξερω τι κανω λαθος και δεν μου βγαινει η σωστη απαντηση που εχει στις λυσεις...
Εχω την αίσθηση ότι ξεχνάς τους συντελεστές στις αντιδράσεις :
Ca(OH) + 2 HCL --> CaCL2 + H2O
Ξαναπροσπάθησε και πές μου ( αντιδρούν 4*10^-3 mol HCL ... )
3. Υδ/κο δ/μα Δ1 εχει ογκο 200 ml και περιεχει 12 g κορεσμενου μονοκαρβοξυλικου οξεος RCOOH.Σε 100 ml του Δ1 διαλυονται 0,05 mol NAOH χωρις μεταβολη του ογκου οποτε προκυπτει Δ2 με ph = 5. α) ποιος ο συντακικος τυπος του RCOOH ; β) το Ph του δ1 ; γ) Στα υπόλοιπα 100 Ml το Δ1 διαλυονται 1,2 g Mg χωρις μεταβολη του ογκου οποτε προκυπτει Δ3. να υπολογισετε : 1. τον ογκο του αεριου που ελευθερωνετε μετρημενο σε συνθηκες STP . 2. To ph του Δ3.
ka RCOOH= 10^-5
κυριως το γ2 ερωτημα ..
σε ολα δινετε η kw = 10^-14 και ηθερμοκρασια 25 βαθμοι κελσιου
Ευχαριστω παρα πολυ προκαταβολικα!!
Μάλλον κάνεις το ίδιο λάθος : Mg + 2 RCOOH --> (RCOO)2Mg + H2 ....
Μετά την περίσσεια πρόσεξε τον συντελεστή στην διάσταση του αλατιού : (RCOO)2Mg --> 2 RCOO- + Mg+2
ΠΡΟΣΟΧΗ ... Η αντιδράσεις με συντελεστές είναι ΣΟΣΑΡΑ για φέτος .... τους περιμέναμε ΚΑΙ πέρισυ αλλά έπεσαν μόνο στα επαναληπτικά ...
2. Υδατικο δ/μα Δ1 ασθενους μονοπρωτικου οξεος ΗΑ εχει [Α- ] = 10 ^-3 Μ . α) ποιος ειναι ο βαθμος ιοντισμου του ΗΑ στο Δ1. Β) σε 200 ml του Δ1 διαλυεται αεριο HCL χωρις μεταβολη του ογκου οποτε προκυπτει Δ2 στο οποιο ισχυει [Α- ] = 10 ^-5 . Να υπολογισετε το PH του Δ2. γ ) Στο Δ2 προστιθενται 400 ml υδατικου δ/τος NAOH με PH=13 και το δμα που προκυπτει αραιωνετε με νερο σε τελικο ογκο 2L ( Δ3). Να υπολογισετε το PH του δ/τος Δ3 και τις συγκεντρωσεις ολων των ιοντων σε αυτο΄. ka HA = 10 ^-5
το γ ερωτημα..
Καλά μιλάμε ... είσαι μέσα στις ΣΟΣΑΡΕΣ ....
Κατά την εξουδετέρωση ενός μίγματος που αποτελείται από ένα ισχυρό και ένα ασθενές οξύ - που έχουν ίδια τάξη συγκεντρώσεων - θεωρούμε ( χωρίς να απέχουμε πολύ από αυτό που συμβαίνει στην πραγματικότητα ) ότι η ποσότητα βάσης που εξουδετερώνει το μίγμα καταναλώνεται πρώτα στην εξουδετέρωση της ποσότητας του ισχυρού οξέος και μετά στην εξουδετέρωση της ποσότητας του ασθενούς οξέος.
Εξουδετέρωσε πρώτα την ποσότητα του HCl και μετά ότι ποσότητα NaOH μείνει , χρησιμοποίησε την για την εξουδετέρωση του ΗΑ ...
Σημείωση: Το μήνυμα αυτό γράφτηκε 11 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
-
Το forum μας χρησιμοποιεί cookies για να βελτιστοποιήσει την εμπειρία σας.
Συνεχίζοντας την περιήγησή σας, συναινείτε στη χρήση cookies στον περιηγητή σας.
 Αρχική Forum
Αρχική Forum
 Ρωτήστε κάτι
Ρωτήστε κάτι
 Προσωπικές Συζητήσεις
Προσωπικές Συζητήσεις
 Πανελλαδικές
Πανελλαδικές
 Αγγελίες
Αγγελίες
 Συνδεδεμένοι Χρήστες
Συνδεδεμένοι Χρήστες
 Λίστα Αποκλεισμένων
Λίστα Αποκλεισμένων
 Υπεύθυνοι του Forum
Υπεύθυνοι του Forum
 e-steki
e-steki