strsismos88
Νεοφερμένος


Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Καλα δε πιστευω να πεσει η ιδια στις εξετασεις, αλλα απο την αλλη αν δε μαθω θα σκασω. Παντως προχωρησα στην υλη, ηταν και η μοναδικη ως τωρα που αφησα αλυτη.βασικα V1 και V2 για αυτον ειναι ο,το το χ και ψ για μενα δεν κολλαμε εκει...το 0,1 ειναι ειπαμε επειδη η βάση ειναι ισχρη με ρΗ 13 απο κει και περα ομως πως δουλευει...?αντιδρα η βαση του στο διαλυμα της πριν τα αναμιξει η εχει το νερο και τα προσθετει...?κι εστω οτι αντιδρα πρωτα η βαση που εγω εβαλα Β- και διισταται πληρως σε ΟΗ- αφου ειναι ισχυρη...το ΗΑ αφου ειναι ασθενες μασ δινει το δικαιωμα να πιστευουμε πως και ι Α- μπορει να αντιδρα με το νερο,αυτο δεν καταλαβαινω.ασ πουμε δηλαδη πως η ισχυρη βαση ειναι ΝαΟΗ,γινεται ολη ΟΗ- και το ασθενες οξυ τυχαια λεω CH3COOH tote kai η A- dld i CH3COO- θα αντιδρα...και παλι επρεπε να βγαινει κανε το πινακακι που εκανα και στην αντιδραση αφαιρεσe τα 0,1V2 mole.Το οξυ ειναι σε περισσεια γιατι εχεισ οξινο ρΗ με ισχυρη βαση.μετα παρε CH3O+=riza KaXcοξεος το Cοξεος ομως ισουται με το C bashs που εφυγε,εχεις και την Κα του HA,kai ti Coksonion apo to pH = 4 ti sto kalo ola ta heis ?tha tin psakso otan vro hrono sou to iposxomai.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Ευχαριστω που ασχοληθηκες φιλε, αλλα καπου κανεις λαθος. Στη λυση βγαινει V1:V2 = 3:10. Γραφει επισης (στη λυση) οτι η αντιδραση που πραγματοποιειται ειναι: HA + OH- --> A- + H3O+. Μετα λεει, ειναι n(HA) = 0,5V1 mol και n(OH-) = 0,1V2 mol. Και τελικα V1:V2 = 3:10ανεβάζω ενα συνημενο δεν ξερω...φαίνεται?
Προσωπικα δε βγαζω νοημα απο τη λυση. Αυτη η ασκηση ειναι στο βοηθημα του Σαββαλα ακριβως πριν το κεφαλαιο των ρυθμιστικων, στην εκδοση μου η τελευταια.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Ευχαριστω!!Καταρχην βρίσκεις την συκεντρωση του δ/τος HCl που ειναι ιση με την [H3O] στο δ/μα γιατι ειναι ισχυρο.Αρα ειναι 0,1 η συγκεντρωση.
Γινεται αντιδραση: NaA + HCl --> HA + NaCl
Ta mols του ΝaA ειναι n=CV=0,02
και του HCl είναι 0,1V
ΜΕ διερευνυση βρισκεις οτι σε περισσεια ειναι το HCl και στο τελικο δ/μα έχεις [ΗCl]=και [ΗΑ]=
Αρα στο τελικο δ/μα εχεις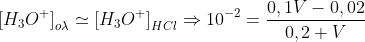
Καμια ιδεα για αυτη την ασκηση υπαρχει? Υδατικο διαλυμα ασθενους οξεος ΗΑ 0,5Μ εχει pH = 2 (Δ1), ενω υδατικο διαλυμα ισχυρης βασης εχει pH = 13 (Δ2). Να υπολογισετε με ποια αναλογια ογκων πρεπει να αναμιξουμε τα διαλυματα Δ1 και Δ2, ωστε να προκυψει διαλυμα Δ3 με pH = 4. Ολα τα διαλυματα εχουν θερμοκρασια 25°C.
Υπολογισα Κα(ΗΑ) = 2*10^-4.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Ολα τα διαλυματα εχουν θερμοκρασια 25°C.
Σημείωση: Το μήνυμα αυτό γράφτηκε 13 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Υδατ. διαλυμα H2SO4 εχει συγκεντρωση 0,5Μ. Να υπολογισετε τις συγκεντρωσεις ολων των ιοντων στο διαλυμα. Δινεται οτι το H2SO4 ιοντιζεται πληρως στο πρωτο σταδιο, ενω στο 2ο στοδιο ειναι Κα2= 1,25 * 10^-2.
Η λυση δινει [SO4^-2] = 0,0125M, [HSO4^-1] ~ 0,5M, [H3O^+1] ~ 0,5M.
Αυτο που με αφορα περισσοτερο ειναι η [SO4^-2], που δε μου βγαινει αυτοματα 0,0125.
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Εγω βγαζω α = 0,5 ενω στη λυση γραφει α = 1/3.
Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
strsismos88
Νεοφερμένος


Σημείωση: Το μήνυμα αυτό γράφτηκε 14 χρόνια πριν. Ο συντάκτης του πιθανόν να έχει αλλάξει απόψεις έκτοτε.
-
Το forum μας χρησιμοποιεί cookies για να βελτιστοποιήσει την εμπειρία σας.
Συνεχίζοντας την περιήγησή σας, συναινείτε στη χρήση cookies στον περιηγητή σας.
 Αρχική Forum
Αρχική Forum
 Ρωτήστε κάτι
Ρωτήστε κάτι
 Προσωπικές Συζητήσεις
Προσωπικές Συζητήσεις
 Πανελλαδικές
Πανελλαδικές
 Αγγελίες
Αγγελίες
 Chat
Chat
 Συνδεδεμένοι Χρήστες
Συνδεδεμένοι Χρήστες
 Λίστα Αποκλεισμένων
Λίστα Αποκλεισμένων
 Υπεύθυνοι του Forum
Υπεύθυνοι του Forum
 e-steki
e-steki